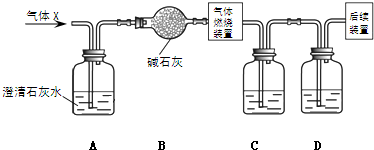
(2013?漳州二模)生铁中含碳和硫等元素.化学兴趣小组对某生铁样品进行了探究.根据要求回答下列问题.生铁中碳和硫元素的定性检验按如图装置进行实验(夹持仪器已略去,填接口字母代号)可以实现碳和硫元素的检验.
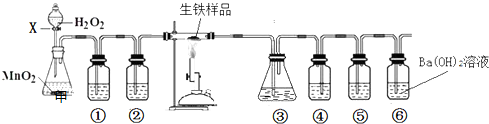
(1)仪器X的名称是
分液漏斗
分液漏斗
;装置③、⑤中试剂相同,装置④中盛放的试剂是
酸性高锰酸钾溶液(或溴水)
酸性高锰酸钾溶液(或溴水)
.
(2)写出甲中反应的化学方程式
.
(3)如果撤除装置③④⑤,能否确认生铁样品中碳元素的存在?
不能
不能
,理由是
SO2也能使氢氧化钡溶液变浑浊
SO2也能使氢氧化钡溶液变浑浊
.
生铁中碳、硫质量分数的测定:
(4)甲同学认为,以上装置可以粗略测定样品中碳的含量.称取样品w
1g进行实验,充分反应后,测得装置⑥中生成的沉淀为w
2g,该样品中碳的质量分数为
(用含w
1、w
2的式子表示).
(5)乙同学认为,待一定量样品充分反应后,向装置④中加入过量氯化钡溶液,根据沉淀质量可以计算样品中硫的质量分数,此方案测得的结果
偏小
偏小
(填“偏大”、“偏小”);若要提高硫元素含量的测定精度,在不改变实验原理的前提下,可以采取的一种措施是
反应结束后,继续同入氧气一段时间且将③中溶液加热到变为红色
反应结束后,继续同入氧气一段时间且将③中溶液加热到变为红色
.

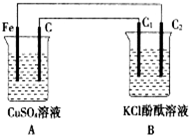 按如图装置进行实验,并回答下列问题(C、C1、C2均为石墨电极).
按如图装置进行实验,并回答下列问题(C、C1、C2均为石墨电极).

 阅读快车系列答案
阅读快车系列答案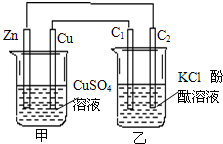 (2010?娄底模拟)(1)以下说法正确的是
(2010?娄底模拟)(1)以下说法正确的是