
| A. | NaNO2是氧化剂 | |
| B. | 每生成1 mol N2时,转移电子数目为6NA | |
| C. | NH4Cl中的氮元素被还原 | |
| D. | N2既是氧化剂,又是还原剂 |
分析 A.化合价降低元素所在的反应物是氧化剂;
B.根据化合价的升降来确定反应中电子的转移;
C.化合价降低元素在反应中被还原;
D.化合价升高元素所在的反应物是还原剂,化合价降低元素所在的反应物是氧化剂.
解答 解:A.反应NaNO2+NH4C1═NaC1+N2↑+2H2O中,NaNO2中N的化合价从+3价降为0价,NaNO2是氧化剂,故A正确;
B.反应NaNO2+NH4C1═NaC1+N2↑+2H2O中,化合价升高值=化合价降低值=转移电子数=3,即每生成1molN2时,转移电子的物质的量为3mol,故B错误;
C.NH4C1中的氮元素化合价从-3价升为0价,所以NH4C1中的氮元素被氧化,故C错误;
D.反应NaNO2+NH4C1═NaC1+N2↑+2H2O中,NaNO2中N的化合价从+3价降为0价,NH4C1中的氮元素化合价从-3价升为0价,氮气既是氧化产物又是还原产物,故D错误;
故选A.
点评 本题考查了氧化还原反应,题目难度不大,氧化还原反应中氧化剂、还原剂的概念以及电子转移知识是重点,考查学生对教材的熟悉程度,试题有利于培养学生的灵活应用能力.


 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:高中化学 来源: 题型:解答题
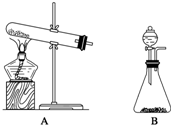 氨气是化学实验室常需制取的气体.实验室制取氨气通常有两种方法:
氨气是化学实验室常需制取的气体.实验室制取氨气通常有两种方法:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 指示剂 | 变色范围 | 酸色 | 碱色 |
| 石蕊 | 5.0-8.0 | 红色 | 蓝色 |
| 酚酞 | 8.0-10.0 | 无色 | 红色 |
| 甲基橙 | 3.1-4.4 | 红色 | 黄色 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
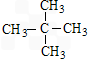 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2F+的电子式: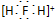 | |
| B. | 铝离子的结构示意图: | |
| C. | 质子数为35、中子数为45的溴原子:${\;}_{35}^{45}$Br | |
| D. | 丙烷分子的球棍模型: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 导致易拉罐变瘪的离子反应是:CO2+OH-═HCO3- | |
| B. | 导致易拉罐又鼓起来的反应是:2Al+2OH-+6H2O═2[Al(OH)4]-+3H2↑ | |
| C. | 若将CO2换为NH3,浓NaOH溶液换为水,易拉罐也会出现先瘪后鼓的现象 | |
| D. | 反应结束后,易拉罐内溶液中的溶质只有Na[Al(OH)4] |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 该烃分子中至少有5个碳原子处于同一直线上 | |
| B. | 该烃分子中所有碳原子可以处于同一平面上 | |
| C. | 该烃分子中至少有12个碳原子处于同一平面上 | |
| D. | 1 mol该烃能与8 mol氢气发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
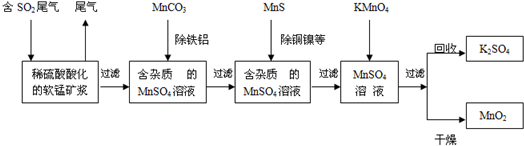
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com