
| A. | 空气中:SO2、NO、N2、NH3 | |
| B. | 明矾溶液中:Na+、K+、CH3COO-、HCO3- | |
| C. | 过量铁与稀硫酸反应后的溶液中:[Fe(CN)6]3-、NH4+、Cl-、NO3- | |
| D. | 常温下,水电离出的c(H+)=1×10-12mol/L的溶液中:Ba2+、Na+、Cl-、NO3- |
分析 A.NO与空气中氧气反应;
B.明矾电离出的铝离子与碳酸氢根离子发生双水解反应;
C.生成的亚铁离子与[Fe(CN)6]3-反应;
D.该溶液中存在大量氢离子或氢氧根离子,四种离子之间不反应,都不与氢离子、氢氧根离子反应.
解答 解:A.NO与空气中氧气反应,在空气中不能大量共存,故A错误;
B.明矾电离出的铝离子与HCO3-发生双水解反应,在溶液中不能大量共存,故B错误;
C.过量铁与稀硫酸反应生成硫酸亚铁和氢气,亚铁离子与[Fe(CN)6]3-反应,在溶液中不能大量共存,故C错误;
D.常温下,水电离出的c(H+)=1×10-12mol/L的溶液中存在大量氢离子或氢氧根离子,Ba2+、Na+、Cl-、NO3-之间不反应,都不与氢离子、氢氧根离子反应,在溶液中能够大量共存,故D正确;
故选D.
点评 本题考查离子共存的正误判断,题目难度中等,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;试题侧重对学生基础知识的训练和检验,有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.


 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:高中化学 来源: 题型:解答题

| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 6.3 | 9.7 |
| Fe3+ | 1.4 | 3.2 |
| Zri2+ | 6.2 | 8.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
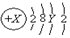 ,则X、Y及该原子3d能级上的电子数不可能的组合是( )
,则X、Y及该原子3d能级上的电子数不可能的组合是( )| A. | 18、8、0 | B. | 20、8、0 | C. | 25、13、5 | D. | 30、18、10 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.2 mol•L-1的NaHCO3溶液中pH>7,则溶液中:c(H2CO3)>c(CO32-) | |
| B. | 叠氮酸(HN3)与醋酸酸性相近,0.1 mol•L-1NaN3水溶液中离子浓度大小顺序为:c(Na+)>c(N3-)>c(OH-)>c(H+) | |
| C. | 向氨水中逐滴滴入盐酸至溶液的pH=7,则混合液中c(NH4+)=c(Cl-) | |
| D. | 0.02 mol/L的NaOH溶液与0.02 mol/L的NaHC2O4溶液等体积混合液:2c(OH-)+c(C2O42-)=c(HC2O4-)+2c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1mol•L-1的三种酸(HA、HB和HD)溶液,滴定的曲线如图所示,下列判断正确的是( )
室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1mol•L-1的三种酸(HA、HB和HD)溶液,滴定的曲线如图所示,下列判断正确的是( )| A. | 室温下,0.1 mol•L-1的三种酸溶液中由水电离产生的c(H+)的关系:HA>HB>HD | |
| B. | 滴定至P点时,溶液中c(B-)>c(Na+)>c(H+)>c(HB)>c(OH-) | |
| C. | pH=7 时,三种溶液中:c(A-)=c(B-)=c(D-) | |
| D. | 当中和百分数达100%时,将三种溶液混合后:c(HA)+c(HB)+c(HD)=c(OH-)-c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.24L(标准状况)苯在O2中完全燃烧,得到0.6NA个CO2分子 | |
| B. | 0.1mol的11B中,含有0.6NA 个中子 | |
| C. | 标准状况下,2.24LN2和O2的混合气体中分子数为0.2NA | |
| D. | 常温常压下,17g 羟基含有的电子总数为 7 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0mol,1mol | B. | 0.5mol,0mol | C. | 0.25mol,.0.5mol | D. | 0.25mol,0.25mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com