
| A. | 甲烷、乙烯 | B. | 乙烷、乙烯 | C. | 乙烷、丙烯 | D. | 甲烷、丙烯 |
分析 根据混合气体的密度是相同状况下H2密度的14.5倍可以确定有机物的平均摩尔质量29g/mol,故混合气体中一定有甲烷,混合气体的总的物质的量为:$\frac{11.6g}{29g/mol}$=0.4mol;该混合气通过Br2水时,Br2水增重8.4g,8.4g为烯烃的质量,所以甲烷的质量为11.6g-8.4g=3.2g,物质的量为0.2mol,故烯烃的物质的量为0.2mol,结合烯烃的质量和物质的量来确定烯烃的摩尔质量,再根据烯烃组成通式确定烯烃.
解答 解:混合气体的密度是相同状况下H2密度的14.5倍,所以混合物的平均摩尔质量为14.5×2g/mol=29g•mol-1,所以混合气体中一定有甲烷,混合气体的总的物质的量为:$\frac{11.6g}{29g/mol}$=0.4mol,该混合气通过Br2水时,Br2水增重8.4g,8.4g为烯烃的质量,所以甲烷的质量为11.6g-8.4g=3.2g,甲烷的物质的量为:$\frac{3.2g}{16g/mol}$=0.2mol,
故烯烃的物质的量为:0.4mol-0.2mol=0.2mol,所以M(烯烃)=$\frac{8.4g}{0.2mol}$=42g•mol-1,
设烯烃的组成为CnH2n,则:14n=42,解得:n=3,故该烯烃为丙烯,
所以该混合物为甲烷、丙烯,
故选D.
点评 本题考查混合物反应的计算、有机物分子式的确定,题目难度中等,根据平均摩尔质量确定含有甲烷是解题的关键,试题培养了学生的分析能力及化学计算能力.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 甘油作护肤保湿剂是因为甘油有还原性 | |
| B. | 服用铬含量超标的药用胶囊会对人对健康造成危害 | |
| C. | “血液透析”利用了胶体的性质 | |
| D. | 葡萄中的花青素在碱性环境下显蓝色,故可用苏打粉检验假红酒 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 操作及现象 | 结论 | |
| A | 向PbSO4悬浊液中加入KI溶液时出现黄色沉淀 | Ksp(PbI2)<Ksp(PbSO4) |
| B | 向某溶液中滴加氯水后再加入稀C6H5OH溶液,溶液呈红色 | 原溶液中可能含有Fe2+ |
| C | 向Na2SiO3溶液中通入过量SO2气体 | 反应为:SiO${\;}_{3}^{2-}$+SO2+H2O=H2SiO3↓+SO${\;}_{3}^{2-}$ |
| D | 将氢气还原氧化铜所得的红色固体加入足量稀硝酸中,溶液变为蓝色 | 反应为:3Cu+2NO${\;}_{3}^{-}$+8H+=3Cu2++2NO↑+4H2O |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “梨花淡自柳深青,柳絮飞时花满城”中柳絮的主要成分和棉花的相同 | |
| B. | 制作烟花的过程中常加入金属发光剂和发色剂烟花放出五彩缤纷的颜色 | |
| C. | 草莓棚中使用的“吊带式二氧化碳气肥”的主要成分可以是碳酸钙 | |
| D. | 《本草纲目》记载的“凡酸坏之酒,皆可蒸烧”的实验方法可用来分离乙酸和乙醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
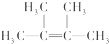 名称为2,3-二甲基-2-丁烯.
名称为2,3-二甲基-2-丁烯.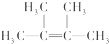 +Br2→
+Br2→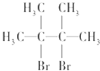 .
.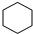 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ,
,查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在50g质量分数为46%的乙醇水溶液中,含有氢原子数为3NA | |
| B. | 80℃时,pH=13的Ba(OH)2溶液中含有的OH-数目为0.2NA | |
| C. | lmol有机物CH3-CH=CH-CH2-CH3中最多有9NA个原子在同一平面上 | |
| D. | l04g苯乙烯(C6H5-CH=CH2)中含有8NA的碳氢键和4NA的碳碳双键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com