

分析 (1)分离不溶性固体和溶液采用过滤的方法、根据同一溶质在不同溶剂中的溶解度采用萃取的方法分离;分液漏斗需要检查上口玻璃活塞处和下口玻璃活塞处是否漏水,采取倒立、放液、旋转倒立等操作
(2)根据仪器的作用选取仪器;
(3)萃取剂的选取标准:萃取剂和原溶剂不互溶,溶质在萃取剂中的溶解度大于在原溶剂中的溶解度,萃取剂和溶质不反应;
(4)进行上述蒸馏操作时,最后晶体碘在蒸馏烧瓶里聚集;
(5)加热蒸馏烧瓶需要垫石棉网;温度计测量馏分的温度;冷凝管中的进水口是下口.
解答 解:(1)分离不溶性固体和溶液采用过滤的方法、根据同一溶质在不同溶剂中的溶解度采用萃取的方法分离,所以①的操作名称是过滤、②的操作名称是萃取和分液,
故答案为:过滤;萃取和分液;关闭分液漏斗颈部旋塞,向分液漏斗内注入适量的蒸馏水,观察旋塞的两端以及漏斗的下口处是否漏水,若不漏水,关闭上磨口塞,左手握住旋塞,右手食指摁住上磨口塞,倒立,检查是否漏水;若不漏水,正立,将上磨口塞旋转180度,倒立,检查是否漏水,若不漏水,则此分液漏斗可以使用;
(2)灼烧海藻时,除需要三脚架外,还需要用到的仪器盛放海藻的坩埚、支撑坩埚的泥三角、用于加热的酒精灯,故选BDE,
故答案为:BDE;
(3)萃取剂的选取标准:萃取剂和原溶剂不互溶,溶质在萃取剂中的溶解度大于在原溶剂中的溶解度,萃取剂和溶质不反应,
A.酒精和水互溶,所以不能作萃取剂,故A错误;
B.四氯化碳、苯与水不互溶,且碘在这两种溶剂中的溶解度比在水中的大,和碘也不反应,故B正确;
C.苯与水不互溶,且碘在这两种溶剂中的溶解度比在水中的大,和碘也不反应,故C正确;
故答案为:BC;四氯化碳、苯与水不互溶,且碘在这两种溶剂中的溶解度比在水中的大,和碘也不反应;
(4)四氯化碳沸点:76.8℃,碘单质沸点为184℃,故最后晶态碘在蒸馏烧瓶里聚集,
故答案为:蒸馏烧瓶;
(5)为了时蒸馏烧瓶受热均匀,则加热蒸馏烧瓶需要垫石棉网;温度计测量馏分的温度而不是溶液的温度;为防止蒸气急剧冷却而炸裂冷凝管,则冷凝管中的进水口是下口,
故答案为:未垫石棉网,应该垫石棉网;温度计的水银球不应插在溶液中,应该处于蒸馏烧瓶的支管口处;冷凝管水流方向错了,下口为进水口.
点评 本题考查了海水资源的综合利用,涉及基本操作、实验仪器的选取、萃取剂的选取标准等知识点,明确实验原理是解本题关键,根据基本操作方法、仪器的作用、萃取剂的特点等知识点来分析解答,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | ①②③⑤ | B. | ①②④⑥ | C. | ②③④⑤ | D. | ③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
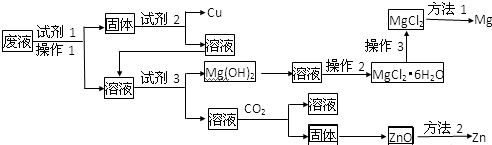
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 准确量取20.00mL高锰酸钾溶液,可选用25mL碱式滴定管 | |
| B. | 将水加热,Kw增大,pH不变 | |
| C. | 用惰性电极电解1L浓度均为2mol/L的AgNO3与Cu(NO3)2的混合溶液,当有0.2 mol 电子转移时,阴极析出6.4g金属 | |
| D. | NaAlO2的水溶液经加热浓缩、蒸干灼烧后能得到NaAlO2固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸发时将蒸发皿放置在铁架台的铁圈上,并加垫石棉网加热 | |
| B. | 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 | |
| C. | 铝箔在酒精灯火焰上加热熔化但不滴落,说明铝箔表面氧化铝膜的熔点高于铝 | |
| D. | 向某溶液中加入NaOH溶液得白色沉淀,又观察到沉淀颜色逐渐变为红褐色,说明该溶液中只含有Fe2+,不含有Mg2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3.2g氧气所含氧分子数为0.2NA | |
| B. | 1L0.1mol/L NaCl 溶液中所含的Na+为0.1NA | |
| C. | 0.012 kg 12C中含有碳原子数约为NA | |
| D. | 24g镁变成镁离子时失去的电子数为2N A |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③④⑤ | B. | ②③④ | C. | ①③④⑥ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
| 化学式 | ①H2SO4 ②HNO3 | ③NaOH ④KOH | ⑤Na2SO4 ⑥K2SO4 | ⑦SO2 ⑧SO3 | ⑨NH3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com