
【题目】汽车用汽油的抗爆剂约含 17%的 1,2一二溴乙烷。某学习小组用下图所示装置制备少量 1,2 一二溴乙烷,具体流秳如下: 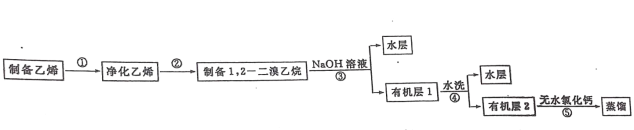
已知:1,2 一二溴乙烷的沸点为131℃,熔点为9.3℃。Ⅰ1,2 一二溴乙烷的制备步聚①、②的实验装置为:
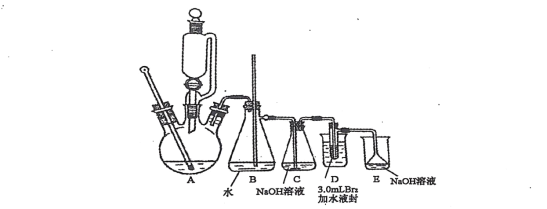
实验步骤:
(ⅰ)在冰水冷却下,将 24mL 浓硫酸慢慢注入12mL乙醇中混合均匀。
(ⅱ)向 D 装置的试管中加入3.0mL 液溴(0.10mol),然后加入适量水液封,幵向烧杯中加入冷却剂。
(ⅲ)连接仪器并检验气密性。向三口烧瓶中加入碎瓷片,通过滴液漏斗滴入一部分浓硫酸与乙醇的混合物,一部分留在滴液漏斗中。
(ⅳ)先切断瓶C与瓶D的连接处,加热三口瓶,待温度上升到约120℃,连接瓶 C与瓶D,待温度升高到180~200℃,通过滴液漏斗慢慢滴入混合液。
(V)继续加热三口烧瓶,待D装置中试管内的颜色完全褪去,切断瓶C与瓶D的连接处,再停止加热。回答下列问题:
(1)图中 B 装置玻璃管的作用为__________________________________________。
(2)(ⅳ)中“先切断瓶C与瓶D的连接处,再加热三口瓶”的原因是__________________________________________。
(3)装置D的烧杯中需加入冷却剂,下列冷却剂合适的为__________________________________________。
a.冰水混合物 b.5℃的水 c.10℃的水
Ⅱ1,2 一二溴乙烷的纯化
步骤③:冷却后,把装置 D 试管中的产物转移至分液漏斗中,用 1%的氢氧化钠水溶液洗涤。
步骤④:用水洗至中性。
步骤⑤:“向所得的有机层中加入适量无水氯化钙,过滤,转移至蒸馏烧瓶中蒸馏,收集
130~132℃的馏分,得到产品5.64g。
(4)步骤③中加入 1%的氢氧化钠水溶液时,发生反应的离子方程式为__________________________________________。
(5)步骤⑤中加入无水氯化钙的作用为_________________________。该实验所得产品的产率为__________________________________________。
【答案】指示 B 中压强变化,避免气流过快引起压强过大 防止乙烯生成前装置中的热气体将溴吹出而降低产率 c Br2+2OH-=Br-+BrO-+H2O 干燥产品(除去产品中的水) 30%
【解析】
(1)图中B装置气体经过,但B中气体流速过快,则压强会过大,通过观察B中玻璃管可以看出气体的流速和反应速率,因此玻璃管的作用为指示B中压强变化,避免气流过快引起压强过大。
(2)(ⅳ)中“先切断瓶C与瓶D的连接处,再加热三口瓶”的原因是防止乙烯生成前装置中的热气体将溴吹出而降低产率。
(3)装置D的烧杯中需加入冷却剂,因为1,2一二溴乙烷的沸点为131℃,熔点为9.3℃,因此只能让1,2一二溴乙烷变为液体,不能变为固体,变为固体易堵塞导气管,因此合适冷却剂为c。
(4)步骤③中加入1%的氢氧化钠水溶液主要是将1,2一二溴乙烷中的单质溴除掉,发生反应的离子方程式为Br2+2OH-=Br-+BrO-+H2O。
(5)步骤⑤中加入无水氯化钙的作用为干燥产品(除去产品中的水);单质溴为0.1mol,根据质量守恒得到1,2一二溴乙烷理论物质的量为0.1mol,因此该实验所得产品的产率为![]() 。
。
(1)图中B装置气体经过,但B中气体流速过快,则压强会过大,通过观察B中玻璃管可以看出气体的流速和反应速率,因此玻璃管的作用为指示B中压强变化,避免气流过快引起压强过大,故答案为:指示B中压强变化,避免气流过快引起压强过大。
(2)(ⅳ)中“先切断瓶C与瓶D的连接处,再加热三口瓶”的原因是防止乙烯生成前装置中的热气体将溴吹出而降低产率,故答案为:防止乙烯生成前装置中的热气体将溴吹出而降低产率。
(3)装置D的烧杯中需加入冷却剂,因为1,2一二溴乙烷的沸点为131℃,熔点为9.3℃,因此只能让1,2一二溴乙烷变为液体,不能变为固体,变为固体易堵塞导气管,因此合适冷却剂为c,故答案为:c。
(4)步骤③中加入1%的氢氧化钠水溶液主要是将1,2一二溴乙烷中的单质溴除掉,发生反应的离子方程式为Br2+2OH-=Br-+BrO-+H2O,故答案为:Br2+2OH-=Br-+BrO-+H2O。
(5)步骤⑤中加入无水氯化钙的作用为干燥产品(除去产品中的水);单质溴为0.1mol,根据质量守恒得到1,2一二溴乙烷理论物质的量为0.1mol,因此该实验所得产品的产率为![]() ,故答案为:干燥产品(除去产品中的水);30%。
,故答案为:干燥产品(除去产品中的水);30%。


科目:高中化学 来源: 题型:
【题目】碳、氢、氧三种元素组成的有机物A,相对分子质量为152,其分子中碳、氢原子个数比为1:1,含氧元素的质量分数为31.58%。A遇FeCl3溶液显紫色,其苯环上的一氯取代物有两种,请回答下列问题:
(1)A的分子式是__。
(2)写出A与NaHCO3溶液反应的化学方程式:__。
(3)若A可以发生如图所示转化关系,D的分子式为C10H12O3,写出D的结构简式__。

(4)甲、乙两装置均可用作实验室由C制取B的装置,乙图采用甘油浴加热(甘油沸点290℃,熔点18.17℃),当甘油温度达到反应温度时,将盛有C和浓硫酸混合液的烧瓶放入甘油中,很快达到反应温度。甲、乙两装置相比较,乙装置有哪些优点___?

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下用pH为3的某酸溶液分别与pH都为11的氨水、氢氧化钠溶液等体积混合得到a、b两种溶液,关于这两种溶液酸碱性的描述正确的是![]()
![]()
A.b一定显中性B.b可能显碱性或酸性
C.a不可能显酸性D.a可能显酸性或碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分枝酸可用于生化研究。其结构简式如图。下列关于分枝酸的叙述正确的是

A. 分子中含有2种官能团
B. 可与乙醇、乙酸反应,且反应类型相同
C. 1mol分枝酸最多可与3molNaOH发生中和反应
D. 可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组查阅资料,设计以下流程验证 SO2 的还原性。
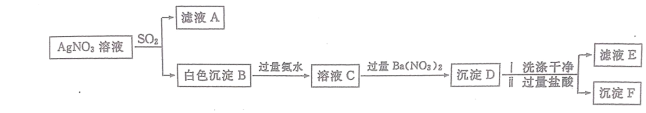
已知:沉淀 D 洗涤干净,加入过量盐酸时,部分沉淀溶解,剩余少量沉淀 F。(1)关于“白色沉淀 B”的成份
①甲同学推断白色沉淀 B 含 Ag2SO4。
实验现象依据:“沉淀 F”说明“沉淀 D”中含________________ (填化学式),进而说明“白色沉淀B"中含 Ag2SO4。
②乙同学认为“白色沉淀 B”中含有 Ag2SO3。
实验现象依据:“沉淀 D 洗涤干净,加入过量盐酸时,部分沉淀溶解”,溶解的物质为 BaSO3, 进而推断沉淀 B 中含 Ag2SO3。为进一步证实 B 中含有 Ag2SO3,可取少量滤液 E于试管中加入少量________________,有白色沉淀生成。
(2)常温下,Ag2SO4 与 Ag2SO3 中 c(Ag+)与 c(SO32-)的关系如下图所示:
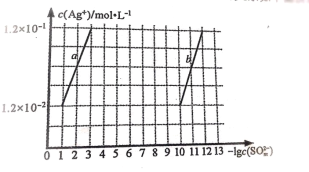
已知:Ksp(Ag2SO4)>Ksp(Ag2SO3),回答问题:
①表示 Ag2SO4 的沉淀溶解平衡关系的曲线是________________ (填“a”、“b”)
②Ksp(Ag2SO3)为________________mol3L-3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,已知某三元弱酸H3A的三级电离平衡常数分别为![]() 、
、![]() 、
、![]() ,下列说法错误的是
,下列说法错误的是
A.Na3A的第一级水解平衡常数Kh1的数量级为10-2
B.在NaH2A溶液中:![]()
C.0.1mol/L的Na3A和0.1mol/L的Na2HA溶液中水电离程度,前者大于后者
D.向H3A溶液中加入NaOH溶液至中性时:c(Na+)=3c(A3-)+2c(HA2-)+c(H2A-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验原理、现象、结论均正确的是( )
A. 图中滴加乙醇,试管中橙色溶液变为绿色,说明
图中滴加乙醇,试管中橙色溶液变为绿色,说明![]() 被还原成
被还原成![]()
B. 图中,右边试管中产生气泡迅速,说明氯化铁的催化效果比二氧化锰好
图中,右边试管中产生气泡迅速,说明氯化铁的催化效果比二氧化锰好
C. 图中,由试管中收集到的无色气体,证明铜与稀硝酸的反应产物是NO
图中,由试管中收集到的无色气体,证明铜与稀硝酸的反应产物是NO
D. 图中,试管中先出现白色沉淀、加
图中,试管中先出现白色沉淀、加![]() 后产生黑色沉淀,但不能验证AgCl的溶解度大于
后产生黑色沉淀,但不能验证AgCl的溶解度大于![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用钛白粉厂废酸(主要含硫酸、Fe3+、Fe2+、TiO2+、Al3+)制备过二硫酸铵[(NH4)2S2O8],同时回收TiO(OH)2的简要流程如下:
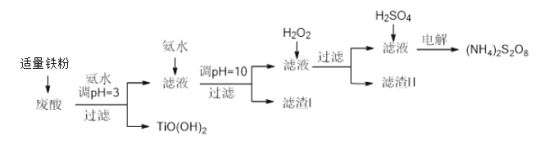
已知:i.部分离子完全生成氢氧化物沉淀的pH:
金属离子 | TiO2+ | Fe3+ | Fe2+ | Al3+ |
开始沉淀的PH | 1.2 | 1.9 | 7.0 | 3.2 |
沉淀完全的pH | 2.8 | 3.1 | 9.4 | 4.7 |
ii.pH>7时,Fe2+部分生成Fe(II)氨络离子[Fe(NH3)2]2+。
请回答下列问题:
(1)加入适量铁的作用是________________________。
(2)生成TiO(OH)2的化学方程式是____________________。
(3)滤渣I、滤渣Ⅱ中均含有的物质的化学式是________
(4)加入H2O2的目的是氧化除掉Fe(II)氨络离子[Fe(NH3)2]2+,配平下列离子方程式:2[Fe(NH3)2]2++____________+4H2O +H2O2=___________+ 4NH3·H2O。
(5)常温下,电解液中含硫微粒主要存在形式与pH的关系如下图所示。
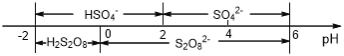
在阳极放电的离子主要为HSO4-,阳极区电解质溶液的pH范围为_________
(6)已知Ksp[Al(OH)3]=3.2×10-34 ,当pH=10 时,求溶液中c(Al3+)=___________
(7)25℃,pH=3的(NH4)2SO4溶液中,计算2c(SO42-)- c(NH4+) =___________(列式即可)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是用于航天飞行器中的一种全天候太阳能电化学电池在光照时的工作原理。下列说法正确的是

A.夜间无光照时,a电极流出电子
B.光照时,H+由a极室通过质子膜进入b极室
C.光照时,b极反应式是VO2++2OH--e-=VO2++H2O
D.该电池与硅太阳能电池供电原理相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com