

���� ������Ҫ�ɷ�ΪB2O3����������Al2O3��SiO2��FeCl3�ȣ�Ϊԭ����ȡNaBH4�������̿�֪����NaOH�ܽ�B2O3��Al2O3��SiO2����FeCl3ת�����������������������1Ϊ���ˣ�����ΪFe��OH��3���ټ�CaO�����������������2ҲΪ���ˣ��Ӷ���ȥ���������Ӧ1ΪNaBO2��MgH2��Ӧ����NaBH4���Դ������
��� �⣺��1��������顢���衢����NaOHŨ�ȡ����µȶ����Լӿ����ܽ����ʣ��ʴ�Ϊ��������顢���衢����NaOHŨ�ȡ����µȣ�
��2���������Ϸ���������1Ϊ���ˣ�������Ҫ�ɷ�ΪFe��OH��3���ʴ�Ϊ�����ˣ� Fe��OH��3��
��3����Ϊ��NaBO2��Һ��ȥ��������NaBO2������ˮ���ڼ����������ȶ����ڣ����Գ������������CaO��������CaCl2��ԭ���У����ܽ��衢���Գ�����ȥ�����ṩ������Һ����NaBO2ˮ�⣬�ʴ�Ϊ���ṩ������Һ����NaBO2ˮ�⣻
��4�����ݻ��ϼ۴�����Ϊ0�����⻯þ��MgH2����HԪ�صĻ��ϼ�Ϊ-1��MgH2��NaBO2��һ�������·�����Ӧ����NaBH4��MgO����Ӧ����ʽΪ��12MgH2+NaBO2=NaBH4+2MgO���ʴ�Ϊ��-1��12MgH2+NaBO2=NaBH4+2MgO��
��5���������ϵ��NaBO2Ҳ���Ƶ����⻯�ƣ���������BO2-�õ��ӷ�����ԭ��Ӧ����BH4-����缫��ӦʽΪ��BO2-+6H2O+8e-=BH4-+8OH-���ʴ�Ϊ��BO2-+6H2O+8e-=BH4-+8OH-��
��6�����⻯����һ��ǿ��ԭ�������������ɴ�����Ʒ�Һ�е�����ͭ�Ƶ�����ͭ����Ӧ�����ӷ���ʽΪ��4Cu2++BH4-+8OH-=4Cu+BO2-+6H2O���ʴ�Ϊ��4Cu2++BH4-+8OH-=4Cu+BO2-+6H2O��
���� ���⿼�����ʵ��Ʊ�ʵ�飬Ϊ��Ƶ���㣬�����Ʊ�ʵ��ԭ����ʵ��װ�õ����á�Ԫ�ػ�����֪ʶΪ���Ĺؼ������ط�����ʵ�������Ŀ��飬ע��Ԫ�ػ�������ʵ�����ϵ�ѵ������Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | C6H6 | B�� | SiO2 | C�� | NaOH | D�� | NH4Cl |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ú�ĸ��� | B�� | ú��Һ�� | C�� | ʯ�ͷ��� | D�� | ʯ���ѻ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
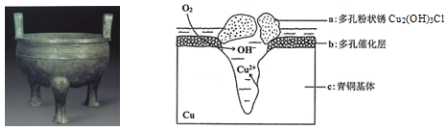
| A�� | ��ͭ�������绯ѧ��ʴ��ͼ��c�������������� | |
| B�� | ���������ĵ缫��ӦΪO2+4e-+2H2O=4OH- | |
| C�� | �����е�Cl-��������������Ӧ�IJ�����������a�����ӷ���ʽΪ2Cu2++3OH-+Cl-=Cu2��OH��3Cl�� | |
| D�� | ������0.2 mol Cu2��OH��3Cl�������������ĵ�O2���Ϊ4.48L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ����I | ����II | �ж� |
| A | ������������������θ����� | Al��OH��3�������ᷴӦ | I�ԣ�II�ԣ��� |
| B | SiO2���������ά | SO2�����õİ뵼�� | I�ԣ�II�ԣ��� |
| C | Al2O3���ͻ���� | Al2O3���и��۵� | I�ԣ�II������ |
| D | HF������ʴ�̲��� | HF��ǿ�� | I�ԣ�II�ԣ��� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2��2-����-3-�һ����� | B�� | 2-��-3-��ϩ | ||
| C�� | 2-��-2-���� | D�� | 2-��-2-��Ȳ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ��֪��CO��g��+2H2��g��?CH3OH��g����H����Ӧ����������1mol CH3OH��g���������仯��ͼ��ʾ�����ߢ�ֱ��ʾ���д�����������������ж���ȷ���ǣ�������
��֪��CO��g��+2H2��g��?CH3OH��g����H����Ӧ����������1mol CH3OH��g���������仯��ͼ��ʾ�����ߢ�ֱ��ʾ���д�����������������ж���ȷ���ǣ�������| A�� | �����������H��С | |
| B�� | ��H=+91 kJ/mol | |
| C�� | ����1molCH3OH��l��ʱ����Hֵ���� | |
| D�� | ��Ӧ�������������������������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com