

| amol��(1-50%) |
| 0.5L |
| 2amol-3��amol��50% |
| 0.5L |
| 2��amol��50% |
| 0.5L |
| c2(NH3) |
| c(N2)��c3(H2) |
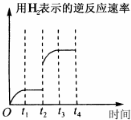 ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��| amol��(1-50%) |
| 0.5L |
| 2amol-3��amol��50% |
| 0.5L |
| 2��amol��50% |
| 0.5L |
| c2(NH3) |
| c(N2)��c3(H2) |
| (2a)2 |
| a��(a)3 |
| 4 |
| a2 |
| 4 |
| a2 |


 �������Ӧ���⼯ѵϵ�д�
�������Ӧ���⼯ѵϵ�д� �ۺ��Բ�ϵ�д�
�ۺ��Բ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ijͬѧ�����һ���ⶨ��Һ�����Ե�ʵ�飨��ͼ��ʾ�������Ȳ�10.0ml 0.10mol/L H2SO4��Һ�ĵ���������Ȼ�������������μ�15.0ml 0.10mol/L Ba��OH��2��Һ�������Ͻ��裮��֪��Һ�е�����Ũ����Ba��OH��2��Һ�������ϵ���£�
ijͬѧ�����һ���ⶨ��Һ�����Ե�ʵ�飨��ͼ��ʾ�������Ȳ�10.0ml 0.10mol/L H2SO4��Һ�ĵ���������Ȼ�������������μ�15.0ml 0.10mol/L Ba��OH��2��Һ�������Ͻ��裮��֪��Һ�е�����Ũ����Ba��OH��2��Һ�������ϵ���£�| Ba��OH��2��ml�� | ��Һ�е�������Ũ�ȣ�mol/L�� |
| 0.0 | 0.30 |
| 5.0 | 0.10 |
| 10.0 | ��0.00 |
| 15.0 | 0.06 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ������ͼװ�ÿ���֤ͬ����Ԫ�طǽ����Եı仯���ɣ�
������ͼװ�ÿ���֤ͬ����Ԫ�طǽ����Եı仯���ɣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Na2A��Һ�Լ��ԣ���NaHA��Һ�����ԣ� |
| B��c��OH-��=c��H+��+c�� HA-��+2c�� H2A�� |
| C��c��Na+ ��+c��H+��=c��OH-��+c�� HA-��+2c��A2-�� |
| D��c��Na+ ��=2c��A2-��+2c�� HA-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����Ƭ���ڲ��ܷ�������� |
| B������������Һʢ������ĥ�ڲ������IJ����Լ�ƿ�� |
| C��Ũ���ᱣ������ɫƿ�����Լ�ƿ�� |
| D��ʵ������ͨ�������������Ʊ�����ú���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���������ˮ��ʳ����Һ�����Բ����κ��Լ� |
| B������Al��OH��3���壨��ɫ����ʳ��ˮ�����Բ����κ��Լ� |
| C������۱�ĩ��ˮ��������ˮ��ɵ���Һ�����Բ����κ��Լ� |
| D������NaCl��CuSO4������Һ�����Բ����κ��Լ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������ظ�������mg����ʱ����������ͬʱ��mg�������� |
| B����ص�������ӦʽΪ��O2ʮ2H2Oʮ4e-=4OH- |
| C������c��Na2CO3����С |
| D�������c��KOH�����䣻��������ҺpH��� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com