
利用催化剂可使NO和CO发生反应:2NO(g)+2CO(g)??2CO2(g)+N2(g) ΔH<0。
已知增大催化剂的比表面积可提高化学反应速率。为了分别验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中。
实验 编号 | T(℃) | NO初始浓度 (mol·L-1) | CO初始浓度 (mol·L-1) | 催化剂的比表 面积(m2·g-1) |
Ⅰ | 280 | 1.2×10-3 | 5.8×10-3 | 82 |
Ⅱ |
| 1.2×10-3 |
| 124 |
Ⅲ | 350 |
|
| 82 |
(1)请填全表中的各空格;
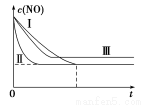
(2)实验Ⅰ中,NO的物质的量浓度(c)随时间(t)的变化如图所示。请在给出的坐标图中画出实验Ⅱ、Ⅲ中NO的物质的量浓度(c)随时间(t)变化的曲线,并标明各曲线的实验编号。

(1)
实验 编号 | T(℃) | NO初始浓度 (mol·L-1) | CO初始浓度 (mol·L-1) | 催化剂的比表 面积(m2·g-1) |
Ⅰ |
|
|
|
|
Ⅱ | 280 |
| 5.8×10-3 |
|
Ⅲ |
| 1.2×10-3 | 5.8×10-3 |
|
(2)
【解析】(1)在其他量相同的情况下,才能判断变量对速率的影响,要验证温度对速率的影响,催化剂的比表面积、反应物的初始浓度等要相同;同理,验证催化剂的比表面积对速率的影响,温度、反应物的初始浓度要相同。
(2)Ⅰ、Ⅱ的区别是催化剂的比表面积不同,因此Ⅱ的反应速率较快,但催化剂不影响平衡的移动。Ⅰ、Ⅲ的区别是温度变化,温度升高,化学反应速率加快,达到平衡的时间缩短,NO转化率降低,故最终Ⅲ中c(NO)较Ⅰ、Ⅱ中c(NO)大。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2014年高考化学一轮复习课后规范训练8-3练习卷(解析版) 题型:填空题
活性ZnO在橡胶、塑料、涂料工业中有重要应用,一种由粗ZnO(含FeO、CuO)制备活性ZnO的流程如下(已知:碱式碳酸锌经焙烧可制得活性ZnO):
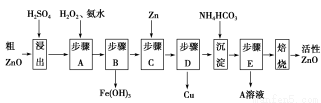
已知:几种离子生成氢氧化物沉淀时的pH如表:
待沉淀离子 | Fe2+ | Fe3+ | Zn2+ | Cu2+ |
开始沉淀时pH | 6.34 | 1.48 | 6.2 | 5.2 |
完全沉淀时pH | 9.7 | 3.2 | 8.0 | 6.4 |
请回答下列问题:
(1)步骤A加H2O2发生反应的离子方程式是 ,该步骤需控制溶液pH的范围是 。
(2)A溶液中主要含有的溶质是 。
(3)碱式碳酸锌经焙烧制得活性ZnO的反应ΔH>0,该反应能自发进行的原因是ΔS (选填“=”、“>”或“<”)0。
(4)若经处理后的废水pH=8,此时Zn2+的浓度为 mg/L(常温下,Ksp[Zn(OH)2]=1.2×10-17)。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练7-3练习卷(解析版) 题型:填空题
甲醇可通过将煤气化过程中生成的CO和H2在一定条件下,发生如下反应制得:CO(g)+2H2(g)  CH3OH(g)。请根据图示回答下列问题:
CH3OH(g)。请根据图示回答下列问题:
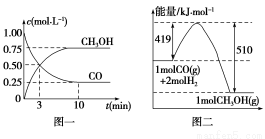
(1)从反应开始到平衡,用H2浓度变化表示平均反应速率v(H2)= ,CO的转化率为 。
(2)该反应的平衡常数表达式为 ,温度升高,平衡常数 (填“增大”、“减小”或“不变”)。
(3)若在一体积可变的密闭容器中充入1 mol CO、2 mol H2和1 mol CH3OH,达到平衡时测得混合气体的密度是同温同压下起始的1.6倍,则加入各物质后该反应向 (填“正”、“逆”)反应方向移动,理由是 。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练7-2练习卷(解析版) 题型:选择题
下列事实不能用勒夏特列原理解释的是( )
①氯化铁溶液加热蒸干最终得不到氯化铁固体
②铁在潮湿的空气中容易生锈
③实验室可用排饱和食盐水的方法收集氯气
④常温下,将1 mL pH=3的醋酸加水稀释至100 mL,测得其pH<5
⑤钠与氯化钾共融制备钾:Na(l)+KCl(l)  K(g)+NaCl(l)
K(g)+NaCl(l)
⑥二氧化氮与四氧化二氮的平衡体系,加压后颜色加深
A.①②③ B.②⑥ C.①③④⑤ D.②⑤⑥
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练7-2练习卷(解析版) 题型:选择题
为了探究外界条件对反应aX(g)+bY(g)  cZ(g)的影响,以X和Y物质的量之比为a∶
cZ(g)的影响,以X和Y物质的量之比为a∶
b开始反应,通过实验得到不同条件下达到平衡时Z的体积分数,实验结果如下图所示。以下判断正确的是( )
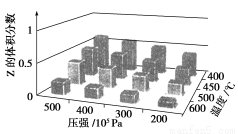
A.ΔH>0,a+b>c B.ΔH>0,a+b<c
C.ΔH<0,a+b>c D.ΔH<0,a+b<c
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练7-1练习卷(解析版) 题型:选择题
在一定条件下的密闭容器中存在下列四个平衡体系,增大容器的体积对化学反应速率没有影响的是( )
A.2SO2+O2 2SO3
2SO3
B.CO+H2O(g) CO2+H2
CO2+H2
C.CO2(g)+H2O H2CO3
H2CO3
D.Fe3++3SCN- Fe(SCN)3
Fe(SCN)3
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练6-1练习卷(解析版) 题型:填空题
当前环境问题是一个全球重视的问题,引起环境问题的气体常见的有温室气体CO2、
污染性气体NOx、SOx等。如果对这些气体加以利用就可以成为重要的能源,既解决了对环境的污染,又解决了部分能源危机问题。
(1)二氧化碳是地球温室效应的罪魁祸首,目前人们处理二氧化碳的方法之一是使其与氢气反应合成甲醇,甲醇是汽车燃料电池的重要燃料。CO2与H2反应制备CH3OH和H2O的化学方程式为
(2)在高温下一氧化碳可将二氧化硫还原为单质硫。
已知:
①C(s)+O2(g)=CO2(g)ΔH1=-393.5 kJ·mol-1
②CO2(g)+C(s)=2CO(g)ΔH2=+172.5 kJ·mol-1
③S(s)+O2(g)=SO2(g)ΔH3=-296.0 kJ·mol-1
请写出CO与SO2反应的热化学方程式 。
(3)硝酸厂常用催化还原方法处理尾气。CH4在催化条件下可以将NO2还原为N2。
已知:CH4(g)+2O2(g)=CO2(g)+2H2O(g)ΔH=-889.6 kJ·mol-1①
N2(g)+2O2(g)=2NO2(g)ΔH=+67.7 kJ·mol-1②
则CH4还原NO2生成水蒸气和氮气的热化学方程式是 。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练5-3练习卷(解析版) 题型:选择题
X、Y为两种短周期元素,其原子的最外层电子数分别是1和6,则X、Y两种元素形
成的常见化合物或者离子不可能是( )
A.只含极性键的共价化合物
B.含非极性键的共价化合物
C.阴阳离子个数之比为1∶1的离子化合物
D.可形成双核离子或者四核离子
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练4-4练习卷(解析版) 题型:实验题
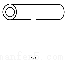
实验室里常见到如图所示仪器,该仪器为两头密封的玻璃管,中间带有一根玻璃短柄。该仪器可进行多项实验,当玻璃管内装有碘晶体时,用此仪器可进行碘升华实验,具有装置简单,操作方便,现象明显,没有污染,可反复使用等优点。
(1)用此仪器不能反复进行的实验是 。
A.NH4Cl固体受热分解
B.KMnO4晶体受热分解
C.白磷和红磷在一定温度下互相转变
(2)如果玻璃管内装有某种红色溶液,加热时溶液颜色变浅,冷却时恢复红色,该溶液可能是 ;如果玻璃管内封有无色溶液,加热溶液时,溶液变红,冷却后恢复原颜色,此溶液可能是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com