
 C(g)+2D(g) ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是
C(g)+2D(g) ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是| A.①② | B.④ | C.③ | D.④⑤ |
科目:高中化学 来源:不详 题型:填空题
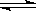 CH3OH(g) ΔH< 0。
CH3OH(g) ΔH< 0。
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.某反应的焓变小于零,该反应一定能自发进行 |
| B.用湿润的pH试纸测稀盐酸溶液的pH为3.52 |
| C.草木灰(K2CO3)是钾肥,硫酸铵是氮肥,二者混合施用可以提高肥效 |
| D.原电池是将化学能转变为电能的装置 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
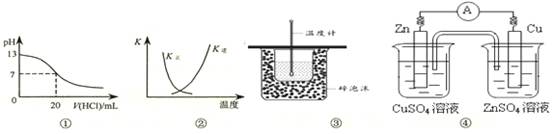
| A.图①表示25℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1 NaOH溶液,溶液的pH随加入酸体积的变化 |
B.图②中曲线表示反应2SO2(g) + O2(g)  2SO3(g);ΔH < 0 正、逆反应的平衡常数K随温度的变化 2SO3(g);ΔH < 0 正、逆反应的平衡常数K随温度的变化 |
| C.图③装置用于测定中和热 |
| D.图④装置可以构成锌、铜、硫酸铜溶液原电池 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①②④⑤ | B.①④⑤⑥ | C.②③⑤⑥ | D.①②④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.无论是风力发电还是潮汐发电,都是将化学能转化为电能 |
| B.在稀溶液中所有酸和碱发生的中和反应的反应热数值都相等 |
| C.化学反应的反应热只与反应体系的始态和终态有关,而与反应的途径无关 |
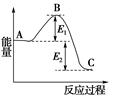
| D.下图中所存在的反应体系,若使用催化剂,E1会减小;若加热升高体系的温度,E1会增加 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
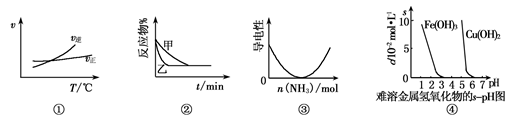
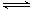 2AB3(g)的ΔH>0
2AB3(g)的ΔH>0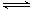 3C(g)的影响,甲的压强大
3C(g)的影响,甲的压强大查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.室温下,向0.01mol·L-NH4HSO4溶液中滴加NaOH 溶液至中性: c(Na+)>c((SO42-)>c(NH4+)>c(OH-)=c(H+) |
| B.0.1mol·L-1NaHCO3溶液:c(Na+)>c(OH-)>c((HCO3-)>c(H+) |
| C.Na2CO3溶液:c(OH-)-c(H+)=c((HCO3-)+2c(H2CO3) |
| D.25℃时,,pH=4.75、浓度均为0.1mol·L-1的CH3COOH 、CH3COONa 混合溶液: |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 图②
图②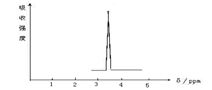
| A.CH3CH3 | B.CH3COOH | C. CH3COOCH3 | D. CH3OCH3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com