
| 20.16L |
| 22.4L/mol |
| 20.16L |
| 22.4L/mol |
| 54g×0.9mol |
| 3mol |
| 16.2g |
| 27g/mol |
| 5mol-2mol-1.8mol |
| 2 |
| 1 |
| 2 |
| ||


科目:高中化学 来源: 题型:
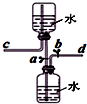
| A、打开止水夹a、b,气体从d管导入,储存在下面的集气瓶里 |
| B、取用储存在下面集气瓶里的气体时,通过控制止水夹a、b |
| C、气体被储存在下面的集气瓶里时,c导管也必须安装止水夹 |
| D、该装置也可作为制取二氧化碳气体的发生装置 |
查看答案和解析>>
科目:高中化学 来源: 题型:
|
|
|
|
| A、A的转化率:甲<丙<乙<丁 |
| B、A的转化率:甲<乙<丙<丁 |
| C、A的转化率:甲<乙=丙<丁 |
| D、B的转化率:甲>丙>乙>丁 |
查看答案和解析>>
科目:高中化学 来源: 题型:
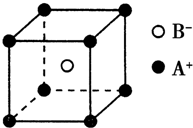
| A、金属键很微弱 |
| B、金属键没有饱和性 |
| C、密堆积层的阳离子容易发生滑动,但不会破坏密堆积的排列方式,也不会破坏金属键 |
| D、金属阳离子之间存在斥力 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在含有Cl-、Br-的混合溶液中加入硝酸银溶液,首先出现的是AgBr沉淀 |
| B、一定温度下物质的溶解度是一定的,所以一定温度下AgCl在水中和在NaCl溶液中的溶解度是一样的 |
| C、AgCl的沉淀溶解平衡方程式为:AgCl(aq)?Ag+(aq)+Cl-(aq) |
| D、将AgCl溶于水形成饱和溶液,过滤得到的饱和溶液中不存在沉淀溶解平衡 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验编号 | HA物质的量浓度(mol?L-1) | NaOH物质的量浓度(mol?L-1) | 混合溶液的pH |
| 甲 | 0.2 | 0.2 | pH=a |
| 乙 | c | 0.2 | pH=7 |
| 丙 | 0.2 | 0.1 | pH>7 |
| 丁 | 0.1 | 0.1 | pH=9 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、泡沫灭火器是最常见的灭火器之一,其内筒为塑料桶,盛有碳酸氢钠溶液;外筒为铁桶,外筒和内筒之间装有硫酸铝溶液 |
| B、“地沟油”经过加工处理后,可以用来制肥皂和生物柴油,可以实现厨余废物合理利用 |
| C、PM2.5受到普遍的关注,因为PM2.5在空气中形成了气溶胶,富含大量的有毒、有害物质,对空气质量影响较大(PM2.5是指大气中直径接近于2.5×10-6m的颗粒物) |
| D、蒙古牧民喜欢用银器盛放鲜牛奶有其科学道理:用银器盛放鲜牛奶,溶入的极微量的银离子,可杀死牛奶中的细菌,防止牛奶变质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
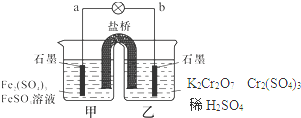
| A、甲烧杯的溶液中发生还原反应 |
| B、乙烧杯中发生的电极反应为:2Cr3++7H2O-6e-=Cr2O72-+14H+ |
| C、外电路的电流方向是从b到a |
| D、电池工作时,盐桥中的SO42- 移向乙烧杯 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com