
【题目】A、B、C、D、E、F是原子序数依次增大的短周期元素。A、B可分别与C组成常见化合物AC、AC2、BC、BC2; 6种元素中原子半径最大的是D元素;E、F两元素单质的沸点与元素原子序数的关系如图(图中原子序数连续)。下列判断与说法正确的是
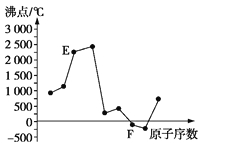
A.元素C、D、F的原子半径由小到大的顺序为F<C<D
B.元素B、E形成的化合物具有类似金刚石的结构,熔点高,硬度大,所以在该化合物中B、E之间存在的是共价键
C.元素A、B、F的最高价氧化物对应的水化物均属于强酸,且元素F的含氧酸具有强氧化性
D.元素C、D、E所组成化合物的水溶液呈碱性,若加入元素E、F所组成化合物的水溶液,会有白色沉淀析出,同时产生大量气体
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】已知:①向KMnO4晶体滴加浓盐酸,产生黄绿色气体;②向FeCl2溶液中通入少量实验①产生的气体,溶液变黄色;③取实验②生成的溶液滴在淀粉KI试纸上,试纸变蓝色。下列判断不正确的是
A.上述实验证明氧化性:MnO4->Cl2>Fe3+>I2
B.实验①中,用160 mL 10 mol/L的高锰酸钾溶液与足量KMnO4充分反应,标准状况下可制得11.2 L的Cl2
C.实验①生成的气体能使湿润的淀粉KI试纸变蓝
D.实验①中要收集纯净干燥的黄绿色气体,应将气体依次通过饱和食盐水和浓硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有常见的A-J物质存在如下转化关系示意图(反应条件己略去),
已知通常情况下A、H 为固态金属单质,B、D为气态非金属单质,E为淡黄色固体,F为无色液体,J为红褐色沉淀.请回答下列问题:
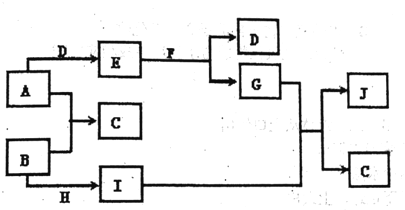
(1)写出下列物质的化学式:A_____;C____; J ______;
(2)转化I+G![]() J+C的反应类型为______。
J+C的反应类型为______。
(3)E中阴阳离子个数比与_______相同(填字母)
a.MgCl2 b.Na2O c.NaCl d.K2SO4
(4)写出下列反应的化学方程式:
① E+F![]() ________;
________;
② B+G![]() _________。
_________。
(5)写出E的一种用途:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组探究在加热条件下FeSO4分解的气体产物及相关性质。已知:SO2的沸点为-10℃、SO3的沸点为44.8℃。
Ⅰ.用如图所示装置设计实验,验证分解FeSO4生成的气态产物。

(1)实验前必须进行的操作是_______________________。
(2)按气流方向连接各仪器,用字母表示接口的连接顺序:a→_________________。
(3)若观察到装置丙中有无色液体产生,装置丁中溶液变成无色,则 FeSO4分解的化学方程式为____________________。
Ⅱ.为探究SO2使品红溶液褪色的原理,进行如下实验:
实验1:将稀盐酸和NaOH溶液分别滴入品红水溶液中。观察到前者溶液颜色变浅,但未能完全褪色,后者溶液颜色几乎不变。
实验2:在滴有稀盐酸和NaOH溶液的两份品红水溶液中分别通入SO2。观察到前者溶液逐渐褪色,后者溶液很快褪色。
实验3:在两份品红水溶液中分别加入一小粒Na2SO3固体和NaHSO3固体,前者溶液很快褪色,后者溶液褪色很慢。
(1)由实验1可推测品红水溶液呈________性。
(2)由实验2、3可推知,使品红水溶液褪色的主要微粒是_________(填化学式)。
(3)若将SO2通入品红的无水乙醇溶液,试预测可能出现的现象________________。
(4)加热溶有Na2SO3的品红水溶液,发现不能恢复红色,试解释原因____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中不正确的是
A. 酸性高锰酸钾溶液可用来鉴别乙烷和乙烯
B. 烃分子中都含有极性键和非极性键
C. ![]() 分子中至少11个碳原子处于同一平面
分子中至少11个碳原子处于同一平面
D. 利用灼烧的方法可鉴别蚕丝和棉制品
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某消毒液的主要成分为NaCl和NaClO,在空气中易吸收CO2而变质,且NaCl和NaClO在酸性条件下可发生反应:ClO- + Cl- + 2H+ = Cl2↑+ H2O。某学习小组拟探究该消毒液的变质情况。
(1)取适量消毒液放在试管中,加入足量一定浓度的硫酸,有气体放出。通过下列装置检验气体的成分可以判断消毒液是否变质。

学习小组研究后认为变质情况可能有三种:甲:部分变质;乙:未变质;丙:______。
为了验证可能为甲,请完成下列实验方案。限选试剂:
a.98%的浓硫酸 b.1%的品红溶液 c.1.0 mol·L-1的KI-淀粉溶液
d.1.0 mol·L-1 的NaOH溶液 e.澄清石灰水 f.饱和NaCl溶液
所加试剂 | 预期现象和结论 |
试管A中加足量______(填序号); 试管B中加1%品红溶液; 试管C中加______(填序号)。 | 若A中________, B中________, C中________,则甲成立。 |
(2)用滴定法测定消毒液中NaClO的浓度。
①在使用滴定管之前首先进行的操作是_____________________;
②量取25.00 mL消毒液放入锥形瓶中,加入过量的a mol·L-1 Na2SO3溶液v1 mL;(反应的化学方程式为:NaClO + Na2SO3 = NaCl+ Na2SO4)将b mol·L-1的用硫酸酸化的KMnO4溶液装入_________(填仪器名称)中;滴定剩余的Na2SO3溶液,反应的化学方程式为:_______________。当溶液由__________(填滴定终点现象)停止滴定,记录数据。
③重复上述滴定操作2次,平均消耗酸性KMnO4溶液v2 mL。则消毒液中NaClO的浓度为_______mol·L-1(用含a、b、v1、v2的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列固体混合物与过量的稀H2SO4反应,能产生气泡并有沉淀生产的是 ( )
A. NaHCO3和Al(OH)3 B. BaCl2和NaCl
C. HClO3和K2SO4 D. Na2SO3和BaCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关C、N、S等非金属元素化合物的说法正确的是( )
A. NaHCO3、Na2CO3、(NH4)2CO3三种固体受热后均能生成气体
B. SO2具有漂白性可以使酸性高锰酸钾溶液褪色
C. 实验室可用NaOH溶液处理NO2和SO2废气
D. 稀硝酸、稀硫酸均能将木炭氧化成二氧化碳
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com