
化学实验中,如果使某步中的有害产物作为另一步的反应物,形成一个循环,就可不再向环境排放该种有害物质。例如:

(1)在上述有编号的步骤中,需用还原剂的是 ,需用氧化剂的是 。(填编号)
(2)在 K2Cr2O7 + 14HCl ==== 2KCl + 2CrCl3 + 3Cl2↑+ 7H2O反应中, 元素被氧化,
==== 2KCl + 2CrCl3 + 3Cl2↑+ 7H2O反应中, 元素被氧化,
是氧化剂;并用双线桥表明电子转移方向与数目: 。
(3)在(2)的反应中,盐酸的作用: 。
23.(1) ① , ④ ;
(2)Cl , K2Cr2O7 ,
 ;
;
(3)酸性与还原性。
【解析】
试题分析:(1)在①变化中,Cr元素由+7价变为+3价,化合价降低,需还原剂;②③两步变化中Cr元素的价态都是+3价,⑤步变化中Cr元素的价态都是+7价,②③⑤都是非氧化还原反应;在④步变化中,Cr元素由+3价变为+7价,化合价升高,需要氧化剂,答案为① ④;
(2)氧化还原反应K2Cr2O7+14HCl═2KCl+2CrCl3+3Cl2+7H2O反应中,化合价升高的元素Cl元素被氧化,对应产物Cl2是氧化产物,化合价降低元素Cr被还原,所在的反应物K2Cr2O7是氧化剂,发生还原反应,用双线桥表明电子转移方向与数目

(3)在氧化还原反应K2Cr2O7+14HCl═2KCl+2CrCl3+3Cl2+7H2O中,盐酸生成KCl,体现酸性,生成氯气,体现还原性,答案为酸性与还原性。
考点:考查化学方程式的配平方法,氧化还原反应的基本概念。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2014-2015学年湖南省浏阳市高一上第一次月考试卷化学试卷(解析版) 题型:选择题
下列括号中的物质是除去杂质所需的药品,其中错误的是 ( )
A.NaCl中有杂质Na2SO4(硝酸钡)
B.FeSO4中有杂质CuSO4(铁粉)
C.O2中有少量HCl气体(氢氧化钠溶液)
D.CO2中有少量CO(灼热的氧化铜)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省高一上学期期中化学试卷(解析版) 题型:选择题
下列操作正确的是
A.给试管内的液体加热,可使试管口对准自己,不能使试管口对准别人
B.用KMnO4制取O2时,先检验装置的气密性,然后再加药品
C.把NaOH固体直接放在天平的左盘上称量
D.稀释浓H2SO4时,可向盛浓H2SO4的量筒中小心加水
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省高一上学期第一次阶段考试化学试卷(解析版) 题型:选择题
下列各组离子在水溶液中能大量共存的是 ( )
A.Na+、Ba2+、Cl?、SO42- B.Ca2+、HCO3?、Cl?、K+
C.Mg2+、Ag+、NO3?、Cl? D.H+ 、Cl? 、Na+ 、CO32?
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省高一上学期第一次阶段考试化学试卷(解析版) 题型:选择题
选择萃取剂将碘水中的碘萃取出来,这种萃取剂应具备的性质是 ( )
A.不溶于水,且必须易与碘发生化学反应
B.不溶于水,且比水更容易使碘溶解
C.不溶于水,且密度必须比水大
D.不溶于水,且密度必须比水小
查看答案和解析>>
科目:高中化学 来源:2014-2015学年辽宁省五校协作体高一上学期期中化学试卷(解析版) 题型:选择题
已知在相同条件下进行下列反应:
①Cl2+2KBr=2KCl+Br2
②KClO3 +6HCl=3Cl2+KCl +3H2O
③2KBrO3 +Cl2=Br2 + 2KClO3,下列说法正确的是
A.上述三个反应都有单质生成,所以都是置换反应
B.反应①和反应③中均生成Br2,溴元素发生的变化相同
C.反应②中被氧化与被还原物质的物质的量之比为6:1
D.③中lmol还原剂反应则氧化剂得到电子的物质的量为10mol
查看答案和解析>>
科目:高中化学 来源:2014-2015学年辽宁省五校协作体高一上学期期中化学试卷(解析版) 题型:选择题
一定量某营养液中溶质的配方分别如下:
配方一:0.3mol KCl,0.2mol K2SO4,0.1 molZnSO4
配方二:0.1 mol KCl,0.3 mol K2SO4,0.1 molZnCl2
对于两种营养液的成分,下列说法中正确的是
A.只有n(K+)相同
B.只有n(Cl-)相同
C.各离子的物质的量完全不同
D.完全相同
查看答案和解析>>
科目:高中化学 来源:2014-2015学年辽宁沈阳铁路实验中学高二上学期第一次月考化学试卷(解析版) 题型:选择题
已知NaHSO4在水中的电离方程式为:NaHSO4=Na++H++SO42-。某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。下列对该溶液的叙述中,不正确的是( )
A.该温度高于25℃
B.由水电离出来的H+的浓度是1.0×10-10mol·L-1
C.NaHSO4晶体的加入抑制了水的电离
D.该温度下加入等体积pH为12的NaOH溶液可使该溶液恰好呈中性
查看答案和解析>>
科目:高中化学 来源:2014-2015学年辽宁大连市高二上期中考试化学试卷(解析版) 题型:填空题
影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究。他们利用Cu、Fe、Mg和不同浓度的硫酸(0.5mol/L、2mol/L、18.4mol/L),设计实验方案来研究影响反应速率的因素。甲同学研究的实验报告如下表:
实 验 步 骤 | 现 象 | 结 论 |
①分别取等体积的2 mol/L硫酸于试管中; ②分别投入大小、形状相同的Cu、Fe、Mg。 | 反应快慢: Mg>Fe>Cu | 反应物的性质越活泼,反应速率越快。 |
(1)该同学的实验目的是 ;
要得出正确的实验结论,还需控制的实验条件是 。
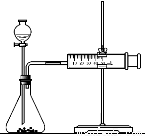
(2)乙同学为了更精确地研究浓度对反应速率的影响,利用下图装置进行定量实验。完成该实验可选用的实验药品是 ;
应该测定的实验数据是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com