
分析 (1)Na2O2投入到AlCl3溶液中,Na2O2和水发生氧化还原反应生成氢氧化钠和氧气,氢氧化钠与氯化铝反应生成氢氧化铝沉淀,氢氧化铝为两性氢氧化物,可与氢氧化钠反应而溶解;
(2)Na2O2投入FeCl2溶液反应中Na2O2和水反应,生成的氢氧化钠和氧气,过氧化钠具有强氧化性,最终生成Fe(OH)3红褐色沉淀.
解答 解:(1)将Na2O2投入AlCl3溶液中,发生的反应为:2Na2O2+2H2O═4NaOH+O2↑,氢氧化钠与氯化铝发生AlCl3+3NaOH=Al(OH)3↓+3NaCl,生成氢氧化铝沉淀,氢氧化钠溶液过量,可氢氧化铝反应而使沉淀溶解,反应的方程式为:Al(OH)3+NaOH=NaAlO2+2H2O,
故答案为:CD;
(2)将Na2O2投入FeCl2溶液中,发生的反应为:2Na2O2+2H2O═4NaOH+O2↑,2OH-+Fe2+═Fe(OH)2↓,由于过氧化钠具有强氧化性,最终生成红褐色的Fe(OH)3沉淀,所以看到的现象是:有大量气泡生成,有红褐色沉淀生成,
故答案为:BC.
点评 本题考查Na2O2的化学性质,注意向溶液中加入Na2O2时,Na2O2先和水反应,然后再发生与其它物质的反应,注意Na2O2的量与AlCl3间的反应关系以及过氧化钠的强氧化性.


科目:高中化学 来源: 题型:选择题
| A. | 向硫酸铝铵溶液中滴加少量Ba(OH)2溶液:NH${\;}_{4}^{+}$+Al3++2SO${\;}_{4}^{2-}$+2Ba2++5OH-═AlO+2BaSO4↓+NH3•H2O+2H2O | |
| B. | 工业上用石灰乳制备漂白粉:Ca(OH)2+Cl2═Ca2++ClO-+Cl-+H2O | |
| C. | 制备Fe(OH)3胶体:Fe3++3H2O?Fe(OH)3(胶体)+3H+ | |
| D. | 用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2═2Mn2++5O2↑+8H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、H+、NO3-、CO32- | B. | Na+、Fe3+、I-、SO42- | ||
| C. | K+、Cu2+、SO42-、OH- | D. | Na+、Fe3+、NO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2F2+2H2O═4HF+O2 | B. | 2Al+2H2O+2NaOH═2NaAlO2+3H2↑ | ||
| C. | 2K+2H2O═2KOH+H2↑ | D. | 2Na2O2+2H2O═4NaOH+O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,pH=5的NaHC2O4溶液中:c(C2O42-)>c(H2C2O4) | |
| B. | 在0.1mol•L-1的CH3COONa溶液中:n(OH-)+0.1mol>n(CH3COOH)+n(H+)+n(Na+) | |
| C. | 向AgBr的饱和溶液中加入NaCl固体,有白色固体析出,说明AgCl比AgBr更难溶 | |
| D. | 10mL0.1mol•L-1H2SO4与10mL 0.01mol•L-1NaOH溶液充分混合,若混合后的体积为20mL,则溶液的pH=7 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 配制标准溶液的氢氧化钠中混有氯化钠杂质 | |
| B. | 滴定终点读数时,俯视滴定管的刻度,其它操作均正确 | |
| C. | 盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗 | |
| D. | 碱式滴定管尖嘴部分的气泡没全部赶跑 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 强弱电解质的区别是溶液的导电能力大小 | |
| B. | 溶液与胶体的本质区别是有无丁达尔效应 | |
| C. | 相同条件下,等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 | |
| D. | 约含6.02×1023个Na+的Na2O2投入水中配成1L溶液,Na+的物质的量浓度为1mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
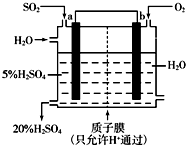 在硫酸工业中,SO2转化为SO3是一个关键步骤
在硫酸工业中,SO2转化为SO3是一个关键步骤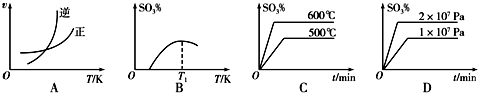
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com