
| A. | 只有③ | B. | 只有① | C. | ①和② | D. | 都正确 |
分析 依据NH3和H2O;NH4+和H3O+;NH2-和OH-;N3-和O2-,每组中的物质性质两两相似,通过对已学过离子的性质和发生的反应推断相应离子的性质,利用类推方法得到答案.
解答 解:①NH4+和H3O+相当,依据CaO+2HCl=CaCl2+H2O;类推得到反应:CaO+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+H2O,故正确;
②NH3和H2O相当,可以依据2Na+2H2O═2NaOH+H2↑,类推得到反应为:2Na+2NH3═2NaNH2+H2↑,故正确;
③OH-和NH2-相当,N3-和O2-两两相当,依据Mg(OH)2=MgO+H2O,类推得到:3Mg(NH2)2$\frac{\underline{\;\;△\;\;}}{\;}$Mg3N2+4NH3↑,故正确;
④OH-和NH2-相当,NH3和H2O相当,依据NH4Cl+NaOH=NaCl+NH3+H2O;类推得到:NH4Cl+NaNH2═NaCl+2NH3,故正确;
故选:D.
点评 本题考查了信息的分析应用,主要考查依据微粒相似,性质相似,依据已学知识类推反应判断,侧重考查学生对所学知识的迁移应用,题目难度中等.


科目:高中化学 来源: 题型:实验题


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 食品袋中常放有硅胶和铁粉,都能起到干燥的作用 | |
| B. | 大力实施矿物燃料脱硫脱硝技术,能减少硫、氮氧化物的排放 | |
| C. | 明矾净水时发生了化学及物理变化,能起到净水作用,而没有杀菌、消毒的作用 | |
| D. | 洗涤脱排油烟机表面的油脂污物时,热的纯碱溶液比冷的去污效果好 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 聚乙烯塑料的老化是由于发生了加成反应 | |
| B. | 乙酸乙酯在碱性条件下的水解反应称为皂化反应 | |
| C. | 葡萄糖注射液不能产生丁达尔效应现象,不属于胶体 | |
| D. | 棉、麻、合成纤维完全燃烧都只生成CO2和H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向Mg(HCO3)2溶液中加入过量的 NaOH溶液:Mg2++2HCO3-+4OH-=Mg(OH)2↓+2CO32-+2H2O | |
| B. | FeBr2溶液中通入等物质的量Cl2:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- | |
| C. | 酸性KMnO4溶液中加H2O2,紫色褪去:2MnO4-+H2O2+6H+=2Mn2++3O2↑+4H2O | |
| D. | 向CuSO4溶液中加入Na2O2:2Na2O2+2Cu2++2H2O=4Na++2Cu(OH)2↓+O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
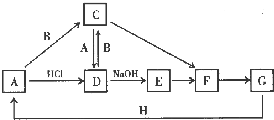 A~H 是中学化学中常见的物质,转化关系如下图所示(部分反应物、反应条件和产物已略去).A、H 是常见的金属单质,工业上常用电解法冶炼H;通常状况下B 为黄绿色气体;G 为红棕色固体;C、D、E、F、G 物种化合物含有同一种元素.
A~H 是中学化学中常见的物质,转化关系如下图所示(部分反应物、反应条件和产物已略去).A、H 是常见的金属单质,工业上常用电解法冶炼H;通常状况下B 为黄绿色气体;G 为红棕色固体;C、D、E、F、G 物种化合物含有同一种元素.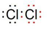 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com