
| A. | 核电荷为12的原子 | B. | 质子数为8的原子 | ||
| C. | K层为最外层时有2个电子的原子 | D. | 核电荷数为9的原子 |
分析 根据原子结构示意图,1个电子层最外层电子数为2,2个或2个以上电子层最外层电子数为8,在化学反应中既不容易得到电子,也不容易失去电子,化学性质稳定来判断.
解答 解:A、因最外层电子数为2,容易失去2个电子达到稳定结构,化学性质不稳定,故A错误;
B、因最外层电子数为6,容易得到2个电子达到稳定结构,化学性质不稳定,故B错误;
C、K层为最外层时有2个电子的原子,则为Ne原子,表示化学性质最稳定的原子,故C正确;
D、因最外层电子数为7,容易得到1个电子达到稳定结构,化学性质不稳定,故D错误;
故选C.
点评 本题考查学生对原子的结构示意图的认识,学生能利用结构示意图来分析最外层电子数并判断其性质,解本题的关键是知道C是稀有气体元素.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ | B. | 2HI$\frac{\underline{\;高温\;}}{\;}$H2+I2 | ||
| C. | H2O+SO2═H2SO3 | D. | Fe2O2+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 反应物的总键能高于生成物的总键能 | |
| B. | 曲线a是使用了催化剂的能量变化曲线 | |
| C. | 热化学方程式为:CO(g)+2H2(g)?CH3OH(g)△H=-91kJ•mol-1 | |
| D. | CO(g)+2H2(g)?CH3OH(1)(g)△H>-91kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
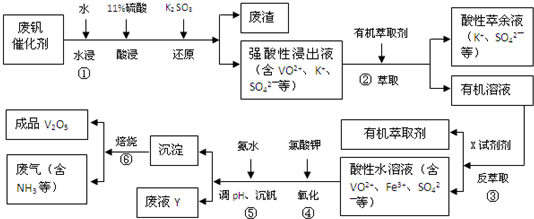
| pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
| 钒沉淀率/% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.8 | 96.4 | 93.1 | 89.3 |
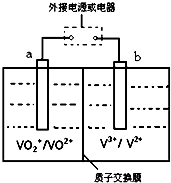
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ;写出其单质的一种重要用途用作半导体材料(或用作太阳能电池板或制作计算机芯片).
;写出其单质的一种重要用途用作半导体材料(或用作太阳能电池板或制作计算机芯片).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,含有的化学键为极性键、非极性键(填“极性键”、“非极性键”、“离子键”).
,含有的化学键为极性键、非极性键(填“极性键”、“非极性键”、“离子键”).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com