
下列有关金属保护方法的说法中正确的是( )
| A.我们使用的快餐杯表面有一层搪瓷,搪瓷层破损后仍能起到防止铁生锈的作用 |
| B.白铁(镀锌铁)镀层破损后,铁皮的腐蚀速率很慢 |
| C.轮船的船壳水线以下常装有一些锌块,这是利用了牺牲阴极的阳极保护法 |
| D.钢铁制造的暖气管道外常涂有一层沥青,这是钢铁的电化学保护法 |
科目:高中化学 来源: 题型:单选题
利用下列装置,可完成很多电化学实验。下列有关叙述,正确的是
| A.若X为锌棒,开关K置于A处,可减缓铁的腐蚀,这种方法称为牺牲阴极的阳极保护法 |
B.若X为铜棒,开关K置于A处,装置中发生的总反应为2NaCl+2H2O 2NaOH+Cl2↑+H2↑ 2NaOH+Cl2↑+H2↑ |
| C.若X为碳棒,开关K置于B处,在铁棒附近滴入铁氰化钾溶液可看到溶液变血红色 |
| D.若X为碳棒,开关K置于B处,向食盐水中滴入酚酞溶液可看到碳棒附近先变红 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
气体的自动化检测中常常应用原电池原理的传感器。下图为电池的工作示意图:气体扩散进入传感器,在敏感电极上发生反应,传感器就会接收到电信号。下表列出了待测气体及敏感电极上部分反应产物。则下列说法中正确的是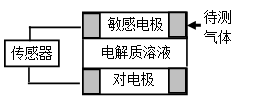
| 待测气体 | 部分电极反应产物 |
| NO2 | NO |
| Cl2 | HCl |
| CO | CO2 |
| H2S | H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
用酸性氢氧燃料电池为电源进行电解的实验装置图如图所示,下列说法中正确的是( )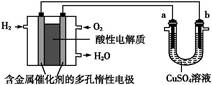
| A.燃料电池工作时,正极反应为:O2+2H2O+4e-=4OH- |
| B.a极是铁,b极是铜时,b极逐渐溶解,a极上有铜析出 |
| C.a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出 |
| D.a、b两极均是石墨时,在相同条件下a极产生的气体与电池中消耗的H2体积相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
以KCl和ZnCl2混合液为电镀液在铁制品上镀锌,下列说法正确的是( )
| A.未通电前上述镀锌装置可构成原电池,电镀过程是该原电池的充电过程 |
| B.因部分电能转化为热能,电镀时通过的电量与锌的析出量无确定关系 |
| C.电镀时保持电流恒定,升高温度不改变电解反应速率 |
| D.镀锌层破损后对铁制品失去保护作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
两种金属A与B组成原电池时,A是正极。下列有关推断正确的是( )
| A.A的金属性强于B |
| B.A电极上发生的电极反应是还原反应 |
| C.电子不断由A电极经外电路流向B电极 |
| D.A在金属活动性顺序表中一定排在氢前面 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
根据图所示装置,下列说法不正确的是( )
| 选项 | 开关状态 | 溶液A | 电极B | 说明 |
| A | 打开K1,闭合K2 | NaCl | 石墨 | 正极反应:O2+2H2O+4e-=4OH- |
| B | 打开K1,闭合K2 | NaCl | Zn | 铁制品保护:牺牲阳极的阴极保护法 |
| C | 打开K2,闭合K1 | CuSO4 | Cu | 铁表面镀铜 |
| D | 打开K2,闭合K1 | CuSO4 | 粗铜 | 电解法精炼铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
有关如图装置的叙述中,正确的是( )
| A.若X为锌棒,Y为NaCl溶液,开关K置于M处,可减缓铁的腐蚀,这种方法称为外接电源的阴极保护法 |
| B.若X为碳棒,Y为饱和NaOH溶液,开关K置于N处,保持温度不变,则溶液的pH保持不变 |
| C.若X为银棒,Y为硝酸银溶液,开关K置于N处,铁棒质量将增加,溶液中银离子浓度将减小 |
| D.若X为铜棒,Y为硫酸铜溶液,开关K置于M处,铜棒质量将增加,此时外电路中的电子向铁电极移动 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com