
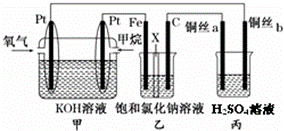
如图所示,某同学设计了一个燃料电池并探究氯碱工业原理的相关问题,其中乙装置中X为阳离子交换膜. 请按要求回答相关问题:
(1)甲烷燃料电池正极反应式为 .
(2)石墨电极(C)的电极反应式为 .
(3)若在标准状况下,有2.24 L氧气参加反应,则乙装置中铁电极上生成的气体体积为 L.
(4)丙中两根铜丝电极的质量均为64g,电解质为500mL 0.1mol•L﹣1H2SO4溶液.电解一段时间后,a端收集到1.12L气体(标准状况下),取出电极,对电极进行干燥并称重,测得b电极的质量减少6.4g.求此时所得溶液的物质的量浓度.
| 原电池和电解池的工作原理. | |
| 专题: | 电化学专题. |
| 分析: | (1)燃料电池中,负极上投放燃料,负极上失电子发生氧化反应; ②甲中投放氧化剂的电极是正极,所以乙装置中铁是阴极,阴极上氢离子得电子发生还有反应; ③根据串联电池中转移电子数相等计算铁电极上生成氢气的体积; (2)根据电解池的工作原理结合电极反应式以及c= |
| 解答: | 解:(1)燃料电池中,负极上投放燃料所以投放甲烷的电极是负极,负极上失电子发生氧化反应,电极反应式为CH4+10OH﹣﹣8e﹣=CO32﹣+7H2O, 故答案为:CH4+10OH﹣﹣8e﹣=CO32﹣+7H2O; ②乙装置中铁是阴极,石墨电极(C)是正极,它的电极反应式为2H++2e=H2↑,故答案为:2H++2e=H2↑; ③串联电池中转移电子数相等,若在标准状况下,有2.24L氧气参加反应,则转移电子的物质的量= 2H++2e﹣=H2↑ 2mol 22.4L 0.4mol xL 解得:x=4.48,故答案为:4.48; (2)电解质为500mL 0.1mol•L﹣1H2SO4溶液,含有氢离子的物质的量是0.1mol,根据通氧气的电极是正极,所以b是阳极,铜丝a是阴极,在a电极上发生电极反应:2H++2e=H2↑,产生0.05mol氢气转移电子是0.1mol,氢离子消耗完毕,在阳极上:Cu﹣2e﹣=Cu2+,减少金属铜6.4g即0.1mol,转移电子是0.2mol,所以在阴极上还会发生反应:Cu2++2e=Cu,再转移0.1mol电子,消耗铜离子0.05mol,所以溶液中铜离子的物质的量是0.1mol﹣0.05mol=0.05mol, 所得硫酸铜溶液的物质的量浓度= |
| 点评: | 本题考查了原电池电极反应式书写、燃料电池电极反应式书写、电解池电极反应式书写,题目难度中等. |


 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:高中化学 来源: 题型:
下列关于热化学反应的描述中正确的是( )
|
| A. | HCl和NaOH反应的中和热△H=﹣57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热△H=2×(﹣57.3)kJ/mol |
|
| B. | CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)═2CO(g)+O2(g)反应的△H=+566.0kJ/mol |
|
| C. | 需要加热才能发生的反应一定是吸热反应 |
|
| D. | 1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
材料的不断发展可以促进社会进步.
①“玉兔”号月球车开创了我国月球表面探索的先河,其制备材料中使用了镁铝合金,选用镁铝合金的优点是 、、 (任答一点).
②碳化硅硬度很大,它属于 (填字母).
a.金属材料 b.无机非金属材料 c.有机高分子材料
③随便丢弃用过的聚乙烯塑料膜会造成白色污染,写出由乙烯在催化剂作用下制备聚乙烯的化学方程式 .

查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,下列溶液的pH或微粒的物质的量浓度关系正确的是( )
|
| A. | Ca(ClO)2溶液中:c(Ca2+)>c(ClO﹣)>c(OH﹣)>c(H﹣) |
|
| B. | 等体积、等物质的量浓度的Na2SO3溶液与NaHSO3溶液混合:c(Na+)=c(SO32﹣)+c(HSO3﹣)+c(H2SO3) |
|
| C. | 将0.2mol.L﹣1的某一元酸HA溶液和0.1mol.L﹣1的NaOH溶液等体积混合后溶液的pH大于7,则反应后的混合液:2c(OH﹣)+c(A﹣)=2c(H+)+c(HA) |
|
| D. | 某溶液中水电离出的c(OH﹣)=1×10﹣amol.L﹣1若a>7时,则pH该溶液的一定为14﹣a |
查看答案和解析>>
科目:高中化学 来源: 题型:
卤素互化物与卤素单质性质相似。已知CH2=CH—CH=CH2(1,3—丁二烯)与氯气发生加成产物有三种:
① CH2Cl—CHCl—CH=CH2 (1,2—加成)
② CH2Cl—CH=CH—CH2Cl (1,4—加成)
③ CH2Cl—CHCl—CHCl—CH2Cl(完全加成)
据此推测CH2=C(CH3)—CH=CH2(异戊二烯)与卤素互化物BrCl的加成产物有几种(不考虑顺反异构和镜像异构( )
A.6种 B.10种 C.12种 D.14种
查看答案和解析>>
科目:高中化学 来源: 题型:
已知A、B、C、D、E五种元素的原子序数依次递增,A、B、C、D位于短周期。A位于周期表的s区,其原子中电子层数和未成对电子数相同;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子最外层电子数是次外层电子数的3倍。E有“生物金属”之称,E4+和氩原子的核外电子排布相同。
请回答下列问题:(1)B、C、D三种元素的电负性由小到大的顺序为 ,E的基态原子的电子排布式为 。(2)由B、D形成的BD32-离子中,其VSEPR模型名称是 ,离子的中心原子采用 杂化。
(3)已知由A、C、D三种元素按照4:2:3的原子个数比可形成某离子化合物,常温下测得该离子化合物的水溶液pH=5,则该溶液中水电离出的氢离子浓度为 。
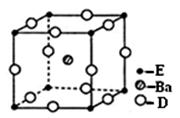 (4)D、E和钡三种元素构成的某化合物的晶胞结构如右图所示,该化合物的化学式为 。纳米级的EO2是一种广泛使用的催化剂,实验室往往通过ECl4在大量水中加热水解制得EO2·xH2O,该反应的化学方程式为 。
(4)D、E和钡三种元素构成的某化合物的晶胞结构如右图所示,该化合物的化学式为 。纳米级的EO2是一种广泛使用的催化剂,实验室往往通过ECl4在大量水中加热水解制得EO2·xH2O,该反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验装置设计正确且能达到目的的是
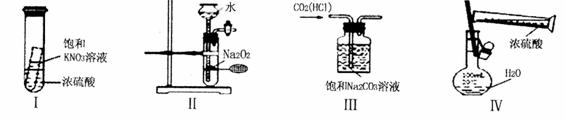
A.实验I:静置一段时间,小试管内有晶体析出 B. 实验II:制取氧气
C. 实验III除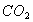 气体中的HCL D.实验IV:配制一定物质的量浓度的稀硫酸
气体中的HCL D.实验IV:配制一定物质的量浓度的稀硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关元素周期表的说法不正确的是 ( )
A.第15列某元素能与其他元素化合形成碱性气体
B.第2列元素中肯定没有非金属元素
C.第17列的第一种元素的原子序数为9
D.短周期中能与强碱反应产生H2的金属元素位于第ⅣA族
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com