
| A. | 1:2 | B. | 8:1 | C. | 1:1 | D. | 80:108 |
分析 在盛有水的电解槽中加入含等物质的量的Ag+,Pb2+,K+,SO42-,NO3-,Br-的物质,充分搅拌,发生的离子反应Ag++Br-=AgBr↓、Pb2++SO42-=PbSO4 ↓,所以溶液中溶质为KNO3,用惰性电极电解该溶液,阳极上氢氧根离子放电,阴极上氢离子放电,则氧化产物是氧气,还原产物是氢气.
解答 解:在盛有水的电解槽中加入含等物质的量的Ag+,Pb2+,K+,SO42-,NO3-,Br-的物质,充分搅拌,发生的离子反应Ag++Br-=AgBr↓、Pb2++SO42-=PbSO4 ↓,所以溶液中溶质为KNO3,用惰性电极电解该溶液,阳极上氢氧根离子放电,阴极上氢离子放电,则氧化产物是氧气,还原产物是氢气,依据化学方程式2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑知,氧化产物和还原产物的物质的量之比为1:2,故选A.
点评 本题考查电解原理和离子共存,为高频考点,正确判断溶液中溶质成分是解本题关键,侧重考查学生分析判断能力,学生在解答过程中易漏掉离子共存而导致错误,为易错题.


 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:解答题

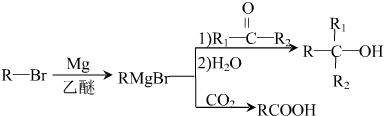
 ,D分子中最多有8个原子共平面.
,D分子中最多有8个原子共平面. (写明反应条件).
(写明反应条件). .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题


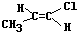 .
. .
.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .过量该物质与偏铝酸钠溶液反应的离子方程式为AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-.
.过量该物质与偏铝酸钠溶液反应的离子方程式为AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A原子的最外层电子数比B原子的最外层电子数少 | |
| B. | 常温时,A能从盐酸中置换出氢气,而B不能反应 | |
| C. | B不能从溶液中置换出A | |
| D. | 1 mol A失去的电子比1 mol B失去的电子多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在金属区、非金属区交界线上,寻找具有半导体性能的材料 | |
| B. | 形成化合物种类最多的元素在第14列 | |
| C. | 第ⅡA族的右边是第ⅢB族,第ⅢA族的左边是第ⅡB族 | |
| D. | 某主族元素最高价氧化物对应的水化物的化学式为HnROm,其气态氢化物的化学式一定为H2m-nR或RH2m-n |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
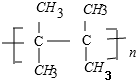 ,A中碳原子是(填“是”或者“不是”)都处在同一平面,A催化加氢后的物质用系统命名法命名名称是2,3-二甲基丁烷;在A的同系物中分子量最小的烃的电子式为CH2=CH2.
,A中碳原子是(填“是”或者“不是”)都处在同一平面,A催化加氢后的物质用系统命名法命名名称是2,3-二甲基丁烷;在A的同系物中分子量最小的烃的电子式为CH2=CH2.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com