
【题目】在密闭容器中进行如下反应:X2(g)+Y2(g) ![]() 2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下,当反应达到平衡时,各物质的浓度有可能是
2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下,当反应达到平衡时,各物质的浓度有可能是
A.Z为0.3mol/L B.Y2为0.4mol/L C.X2为0.2mol/L D.Z为0.4mol/L
【答案】A
【解析】
试题分析:若反应向正反应进行到达平衡,X2、Y2的浓度最小,Z的浓度最大,假定完全反应,则:
X2(气)+Y2(气)2Z(气),
开始(mol/L):0.1 0.3 0.2
变化(mol/L):0.1 0.1 0.2
平衡(mol/L):0 0.2 0.4
若反应逆正反应进行到达平衡,X2、Y2的浓度最大,Z的浓度最小,假定完全反应,则:
X2(气)+Y2(气)2Z(气),
开始(mol/L):0.1 0.3 0.2
变化(mol/L):0.1 0.1 0.2
平衡(mol/L):0.2 0.4 0
由于为可逆反应,物质不能完全转化所以平衡时浓度范围为0<c(X2)<0.2,0.2<c(Y2)<0.4,0<c(Z)<0.4,故A正确、BCD错误.
故选A.


 ABC考王全优卷系列答案
ABC考王全优卷系列答案科目:高中化学 来源: 题型:
【题目】有BaCl2和NaCl混合溶液aL,将它均分成两份。一份滴加硫酸,使Ba2+完全沉淀;另一份滴加AgNO3溶液,使Cl-完全沉淀.反应中消耗xmolH2SO4、ymolAgNO3.据此得知原混合溶液中的c(Na+)为
A. (2y-4x) /amol·L-1 B. (y-2x) /amol·L-1
C. (2y-2x) /amol·L-1 D. (y-x) /amol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷化铝、磷化锌、磷化钙是目前常见的熏蒸杀虫剂,都能与水或酸反应产生有毒气体膦(PH3),PH3具有较强的还原性,能在空气中自燃。卫生安全标准规定,粮食中磷化物(以PH3计)含量≤0.05mg/kg。某化学兴趣小组的同学通过下列方法对粮食中残留磷化物含量进行研究:
【操作流程】安装吸收装置→PH3的产生与吸收→转移KMnO4吸收溶液→亚硫酸标准溶液滴定
【实验装置】

C中盛有200g原粮,D、E、F 各盛装1.00mL浓度为1.00×10-3mol/L的KMnO4 溶液(H2SO4 酸化)。
请回答下列有关问题:
(1)仪器G的名称是 。以磷化铝为例,写出磷化铝与水反应的化学方程式 。
(2)检查C装置气密性的方法是:用止水夹夹紧C装置 ,取下上口活塞,漏斗中加入水,打开下口旋塞,观察到 ,表明装置气密性良好。
(3)实验过程中,用抽气泵反复抽气的目的是 。
(4)A中盛装KMnO4溶液是为除去空气中可能含有的 (填“还原”或“氧化”)性气体;B中盛装新制FeSO4溶液的作用是 ;
(5)已知 D、E、F 中发生同一反应,实验中 PH3被氧化成磷酸,写出所发生的化学反应方程式 ;收集装置D、E、F所得吸收液,并洗涤D、E、F,将吸收液、洗涤液一并置于锥形瓶中,加水稀释至25mL,用浓度为5×10-4 mol/LNa2SO3标准溶液滴定剩余的KMnO4溶液,消耗Na2SO3标准溶液11.00mL,则该原粮中磷化物(以PH3计)的含量为 mg/kg。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学——选修3:物质结构与性质】某配位化合物为深蓝色晶体,由原子序数依次增大的A、B、C、D、E五种元素组成,其原子个数比为l4︰4︰5︰1︰1。其中C、D元素同主族且原子序数D为C的二倍,E元素的外围电子排布为(n-1)d n+6nsl。回答下列问题。
(1)元素D在周期表中的位置是 ,B原子的外围电子排布图为 。E原子的核外有 种不同运动状态的电子,B和C的第一电离能大小关系是 。(用元素符号表示)
(2)C元素可与A元素形成两种常见的化合物,其原子个数比分别为1︰1和l︰2,写出原子个数比为1︰1的化合物的电子式 ,两种化合物可以任意比互溶,解释其主要原因为 。
(3)该配位化合物的化学式为 。
(4)A元素与B元素可形成分子式为A2B2的化合物,该化合物的分子具有平面结构,则其结构式为 ,用电子式表示化合物Na2D的形成过程 。
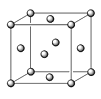
(5)已知E的晶胞结构如图所示,此晶胞立方体的边长为a cm,E单质的密度为ρ g·cm-3,则阿伏伽德罗常数为 (用a、ρ表示)。该晶胞配位数为 ,EDC4常作电镀液,其中DC42-的空间构型是 ,其中D原子的杂化轨道类型是 。若电解EDC4的水溶液,则电解总反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在半导体工业中,有一道工序叫烧氢。烧氢的工艺流程如图所示。
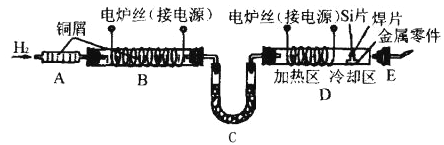
工作时,是将石英管D出口处氢气点燃。半导体硅片、焊片和金属零件从石英管口送入加热区,在氢气还原气氛中加热使焊片熔化,将单晶硅与金属零件焊接在一起。焊接后再将零件拉至冷却区,冷却后取出。烧氢工艺中的氢气纯度要求极高,工业氢气虽含氢量达99.9%,但仍含有极微量的水蒸气和氧气,所以点燃氢气前应检验氢气的纯度。试回答下列问题:
(1)装置B的作用是________;B中发生反应的化学方程式是________。
(2)装置C中的物质是________;C的作用是________。
(3)点燃氢气前将E(带导管胶塞)接在D出口处,目的是________。
(4)装置A是安全瓶,可以防止氢气燃烧回火,引起爆炸,其中填充大量纯铜屑的作用是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将体积为V1的 0.1000mol·L-1HCl 溶液逐滴加入到体积为V2的0.1000mol·L-1Na2CO3溶液中,溶液中H2CO3、HCO3-、CO32-所占的物质的量分数(α)随pH的变化曲线如图。下列说法不正确的是
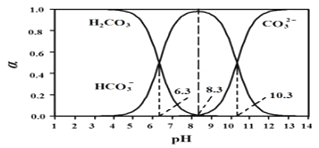
A. 在pH=10.3时,溶液中:c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-)+c(Cl-)
B. 在pH=8.3时,溶液中:0.1000>c(HCO3-)+c(CO32-)+c(H2CO3)
C. 在pH=6.3时,溶液中,c(Na+)>c(Cl-)>c(HCO3-)>c(H+)>c(OH-)
D. V1:V2=1:2时,c(OH-)>c(HCO3-)>c(CO32-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对下列实验现象的解释不正确的是( )
选项 | 实验现象 | 解释 |
A | Cl2使鲜艳的红色花瓣褪色 | Cl2具有强还原性 |
B | NH3与HCl气体接触时有白烟产生 | NH3与HCl反应生成NH4Cl固体小颗粒 |
C | 新切开的Na表面在空气中很快变暗 | Na容易与空气中的氧气等反应 |
D | 加热铝箔时熔化的Al不滴落 | Al表面的氧化膜熔点高,包在熔化的Al外面 |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com