
·ÖĪö £Ø1£©H2£Øg£©+I2£Øg£©ØT2HI£Øg£©”÷H£¼0£®±£³ÖČŻĘ÷ÄŚĘųĢåŃ¹Ēæ²»±ä£¬ĻņĘäÖŠ¼ÓČė1mol N2£¬×ÜĢå»ż±ä“ó£»Ń¹Ēæøı䣬øĆ·“Ó¦ĪŖĢå»ż²»±äµÄæÉÄę·“Ó¦£»
£Ø2£©½«ČŻĘ÷µÄČŻ»żĄ©“óµ½ŌĄ“µÄĮ½±¶£¬ČōĘ½ŗā²»ŅĘ¶Æ£¬AµÄÅضČĪŖ0.25mol/L£¬¶ųŌŁ“ļµ½Ę½ŗāŹ±£¬²āµĆAµÄÅØ¶Č½µµĶĪŖ0.30mol/L£¬æÉÖŖ¼õŠ”Ń¹ĒæĘ½ŗāÄęĻņŅĘ¶Æ£»
£Ø3£©1molæÉČ¼ĪļČ¼ÉÕÉś³ÉĪȶØŃõ»ÆĪļŹ±·Å³öµÄČČĮæĪŖČ¼ÉÕČČ£»
£Ø4£©·“Ó¦A£Øg£©?B£Øg£©+C£Øg£©£¬
æŖŹ¼ n 0 0
×Ŗ»Æ na na na
Ę½ŗā n£Ø1-a£© na na
æÉÖŖA”¢B”¢CĘ½ŗā·ÖŃ¹·Ö±šĪŖ$\frac{£Ø1-a£©p}{£Ø1+a£©}$”¢$\frac{ap}{1+a}$”¢$\frac{ap}{1+a}$£¬ŅŌ“Ė¼ĘĖćKp£»
£Ø5£©µ±¼õŃ¹ŗó»ģŗĻĢåĻµÖŠCµÄ°Ł·Öŗ¬ĮæŌö“ó£¬æÉÖŖ¼õŠ”Ń¹ĒæĘ½ŗāÕżĻņŅĘ¶Æ£¬Ōņm+n£¼p£¬ŌņŌö“óŃ¹ĒæĘ½ŗāÄęĻņŅĘ¶Æ£¬µ«Ģå»żÓ°Ļģø÷ĪļÖŹµÄÅØ¶Č£¬ŅŌ“ĖĄ“½ā“š£®
½ā“š ½ā£ŗ£Ø1£©H2£Øg£©+I2£Øg£©ØT2HI£Øg£©”÷H£¼0£®±£³ÖČŻĘ÷ÄŚĘųĢåŃ¹Ēæ²»±ä£¬ĻņĘäÖŠ¼ÓČė1mol N2£¬×ÜĢå»ż±ä“ó£¬ÅØ¶Č¼õŠ”£¬Ōņ·“Ó¦ĖŁĀŹ¼õŠ”£»øĆ·“Ó¦ĪŖĢå»ż²»±äµÄæÉÄę·“Ó¦£¬Ļąµ±ÓŚ¼õŠ”Ń¹Ē棬¶ųĘ½ŗā²»ŅĘ¶Æ£¬
¹Ź“š°øĪŖ£ŗ±äŠ”£»²»£»
£Ø2£©½«ČŻĘ÷µÄČŻ»żĄ©“óµ½ŌĄ“µÄĮ½±¶£¬ČōĘ½ŗā²»ŅĘ¶Æ£¬AµÄÅضČĪŖ0.25mol/L£¬¶ųŌŁ“ļµ½Ę½ŗāŹ±£¬²āµĆAµÄÅØ¶Č½µµĶĪŖ0.30mol/L£¬æÉÖŖ¼õŠ”Ń¹ĒæĘ½ŗāÄęĻņŅĘ¶Æ£¬ŌņBµÄ×Ŗ»ÆĀŹ±äŠ”£¬CµÄĢå»ż·ÖŹż±äŠ”£¬¹Ź“š°øĪŖ£ŗ±äŠ”£»±äŠ”£»
£Ø3£©ŅŃÖŖ·“Ó¦2CO£Øg£©+O2£Øg£©ØT2CO2£Øg£©”÷H=-566kJ/mol£¬ŌņCOµÄČ¼ÉÕČČĪŖ”÷H=-283kJ/mol£¬¹Ź“š°øĪŖ£ŗ283kJ/mol£»
£Ø4£©·“Ó¦A£Øg£©?B£Øg£©+C£Øg£©£¬
æŖŹ¼ n 0 0
×Ŗ»Æ na na na
Ę½ŗā n£Ø1-a£© na na
æÉÖŖA”¢B”¢CĘ½ŗā·ÖŃ¹·Ö±šĪŖ$\frac{£Ø1-a£©p}{£Ø1+a£©}$”¢$\frac{ap}{1+a}$”¢$\frac{ap}{1+a}$£¬ŌņKp=$\frac{a{\;}^{2}}{1-a{\;}^{2}}$p£¬
¹Ź“š°øĪŖ£ŗ$\frac{a{\;}^{2}}{1-a{\;}^{2}}$p£»
£Ø5£©µ±¼õŃ¹ŗó»ģŗĻĢåĻµÖŠCµÄ°Ł·Öŗ¬ĮæŌö“ó£¬æÉÖŖ¼õŠ”Ń¹ĒæĘ½ŗāÕżĻņŅĘ¶Æ£¬Ōņm+n£¼p£¬Ōņ¼ÓŃ¹ŗó£¬Ę½ŗāĖäÄęĻņŅĘ¶Æ£¬µ«Ģå»ż¼õŠ”£¬CµÄÅØ¶Č±ä“ó£»ČōCŹĒÓŠÉ«ĪļÖŹ£¬A”¢BŹĒĪŽÉ«ĪļÖŹ£¬¼õŠ”Ń¹Ēæ£¬Ę½ŗāÕżĻņŅĘ¶Æ£¬CµÄĪļÖŹµÄĮæŌö“󣬵«Ģå»żŌö“ó£¬æÉÖŖCµÄÅØ¶Č±äŠ”£¬Ōņ·“Ó¦»ģŗĻĪļµÄŃÕÉ«±äĒ³£¬¹Ź“š°øĪŖ£ŗ±ä“ó£»±äĒ³£®
µćĘĄ ±¾Ģāæ¼²é½Ļ×ŪŗĻ£¬Éę¼°»ÆŃ§Ę½ŗā¼ĘĖć¼°»ÆŃ§Ę½ŗāµÄÓ°ĻģŅņĖŲµČ£¬°ŃĪÕĻą¹Ų¼ĘĖć¹«Ź½¼°·“Ó¦ŌĄķĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪö”¢¼ĘĖćÄÜĮ¦µÄ×ŪŗĻ漲飬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½«Ņ»Š”æ齚ŹōÄĘĶ¶ČėĻ”ĮņĖįĶČÜŅŗÖŠ»įÓŠŗģÉ«¹ĢĢåĪö³ö | |
| B£® | Ļņ0.4molÅØŃĪĖįÖŠ¼ÓČė×ćĮæµÄMnO2£¬¼ÓČČ£¬æÉŹÕ¼Æ£Ø±ź×¼×“æöĻĀ£©2.24LCl2 | |
| C£® | Ļņ×ćĮæµÄŃĪĖįŗĶĒāŃõ»ÆÄĘČÜŅŗÖŠø÷¼ÓČėµČÖŹĮæµÄAl·Ū£¬ĻūŗÄŃĪĖįÓėĒāŃõ»ÆÄĘČÜŅŗµÄĪļÖŹµÄĮæÖ®±ČĪŖ3£ŗ1 | |
| D£® | 150 mL 1 mol•L-1NaClČÜŅŗÓė75 mL 1 mol•L-1 Na2CO3ČÜŅŗÖŠNa+ĪļÖŹµÄĮæÅضČĻąµČ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | æÉČ¼±łæÉÄÜŌŚĪ“Ą“Ęū³µ”°Č¼ÓĶ”±Ģę±äĪŖ”°Č¼±ł”± | |
| B£® | æÉČ¼±ł¼“Ź¹æŖ²É²»µ±Ņ²²»»įŌģ³É”°ĪĀŹŅŠ§Ó¦”± | |
| C£® | æÉČ¼±łÖŠÓŠŅ»ÖÖ¼×ĶéĘųĢ壬¼×ĶéŹōĪŽ»śĪļ | |
| D£® | æÉČ¼±łÖŠµÄŅŅĆŃÓėŅŅ“¼»„ĪŖĶ¬·ÖŅģ¹¹Ģå |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŅŅĖįŅŅõ„ÖŠŹĒ·ń»ģÓŠŅŅĖį£¬æÉŅŌ¼ÓŹÆČļŹŌŅŗ½ųŠŠ¼ģ²ā | |
| B£® | ŅŅ“¼ÖŠŹĒ·ń»ģÓŠŅŅĖį£¬æÉŅŌ¼ÓČė½šŹōÄĘ½ųŠŠ¼ģŃé | |
| C£® | ŅŅĖįŅŅõ„”¢ŅŅĖį¾łÄÜÓėNaOH·“Ó¦£¬¶žÕß·Ö×ÓÖŠµÄ¹ŁÄÜĶÅĻąĶ¬ | |
| D£® | µķ·ŪŗĶµ°°×ÖŹ¾łæÉĖ®½āÉś³ÉĘĻĢŃĢĒ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ·“Ó¦4NO2£Øg£©+2NaCl£Øs£©?2NaNO3£Øs£©+2NO£Øg£©+Cl2£Øg£©µÄĘ½ŗā³£ŹżĪŖK12/K2 | |
| B£® | Ę½ŗāŗóc£ØCl2£©=2.5”Į10-2mol/L | |
| C£® | ĘäĖüĢõ¼ž±£³Ö²»±ä£¬·“Ó¦ŌŚŗćŃ¹Ģõ¼žĻĀ½ųŠŠ£¬ŌņĘ½ŗā³£ŹżK2Ōö“ó | |
| D£® | Ę½ŗāŹ±NO2µÄ×Ŗ»ÆĀŹĪŖ50% |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¶žŃõ»ÆĀČ¾ßÓŠĒæŃõ»ÆŠŌ£¬æÉÓĆĄ“ĘÆ°×ÖÆĪļ | |
| B£® | ĀČ»ÆĀĮŹĒĒæµē½āÖŹ£¬æɵē½āĘäĖ®ČÜŅŗ»ńµĆ½šŹōĀĮ | |
| C£® | ŹÆÓ¢ŪįŪöÄĶøßĪĀ£¬æÉÓĆĄ“¼ÓČČČŪ»ÆÉÕ¼ī”¢“æ¼īµČ¹ĢĢå | |
| D£® | ĶµÄ½šŹō»ī¶ÆŠŌ±ČĀĮČõ£¬æÉÓĆĶ¹Ž“śĢęĀĮ¹ŽÖüŌĖÅØĻõĖį |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
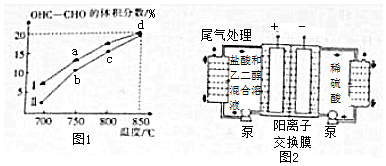
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com