
【题目】在一密闭容器中,反应aA(g)≒bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则( )
A.平衡向正反应方向移动了B.物质A的转化率减少了
C.物质B的质量分数减小了D.a>b
【答案】A
【解析】
采用假设法分析,假设a=b,保持温度不变,将容器体积增加一倍,平衡不移动,A和B的浓度应均是原来的![]() 倍,与达到新的平衡时B的浓度相比判断平衡移动,再根据平衡移动逐项判断。
倍,与达到新的平衡时B的浓度相比判断平衡移动,再根据平衡移动逐项判断。
采用假设法分析,假设a=b,保持温度不变,将容器体积增加一倍,平衡不移动,A和B的浓度应均是原来的![]() 倍,但当达到新的平衡时,B的浓度是原来的60%,说明减小压强平衡向正反应反应方向移动。
倍,但当达到新的平衡时,B的浓度是原来的60%,说明减小压强平衡向正反应反应方向移动。
A、平衡时B的浓度是原来的60%,大于原来的![]() 倍,说明平衡向正反应反应方向移动,选项A正确;
倍,说明平衡向正反应反应方向移动,选项A正确;
B、平衡时B的浓度是原来的60%,大于原来的![]() 倍,说明平衡向正反应反应方向移动,A的转化率增大,选项B错误;
倍,说明平衡向正反应反应方向移动,A的转化率增大,选项B错误;
C、平衡应向正反应方向移动,物质B的质量增多,混合物总质量不变,所以物质B质量分数增大,选项C错误;
D、增大体积,压强减小,平衡向正反应方向移动,则说明a<b,选项D错误。
答案选A。


 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】铝是国民经济发展的重要材料,铝在地壳中的含量约占8%,目前我国铝消费量超过430万吨,在众多的金属中仅次于铁。请回答下问题:
(Ⅰ)实验室中用金属铝制备少量氢氧化铝,有以下3种方案:
方案1:Al![]() Al3+
Al3+![]() Al(OH)3↓
Al(OH)3↓
方案2:Al![]() AlO
AlO![]()
![]() Al(OH)3↓
Al(OH)3↓
方案3: ―→Al(OH)3
―→Al(OH)3
制备相同物质的量的氢氧化铝消耗酸和碱最少的是方案________。
(Ⅱ)工业上冶炼铝的流程图如图所示:

在制取氧化铝的过程中,分析铝土矿和赤泥中所含Al2O3、Fe2O3质量分数的数据如下:

(1)书写化学方程式,反应①________,反应②________。
(2)电解氧化铝生产铝时,阳极的电极反应式为_______________________________________。
(3)假设其他杂质不参加反应,则每生产3.4 t纯净的氧化铝,需铝土矿________t。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式中书写正确的是( )
A. 水玻璃中通入过量的二氧化碳: Na2SiO3+CO2+H2O===2Na++CO![]() +H2SiO3
+H2SiO3
B. 澄清石灰水中通入过量二氧化碳:Ca(OH)2+2CO2===Ca2++2HCO![]()
C. 二氧化硅与氢氟酸反应:SiO2+4H++4F-===SiF4↑+2H2O
D. 二氧化硅溶于烧碱溶液中:SiO2+2OH-===SiO![]() +H2O
+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】判断A(g)+B(g) ![]() C(g)+D(g)是否达到平衡的依据为( )
C(g)+D(g)是否达到平衡的依据为( )
A. 压强不随时间改变
B. 气体的密度不随时间改变
C. c(A)不随时间改变
D. 单位时间里生成C和D的物质的量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“瑞德西韦(Remdesivir)”对新型冠状病毒(SARS-CoV-2)有明显的抑制作用,其合成路线如下:
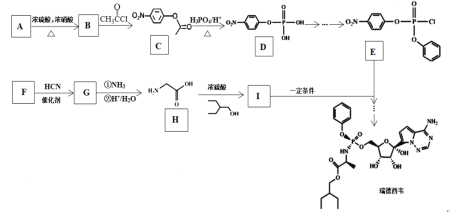
已知:![]()
(1)有机物G中官能团名称是________、_________。
(2)有机物H的化学名称为____________。
(3)A到B的反应类型是___________。
(4)有机物F的结构简式是__________。
(5)写出由B到C的反应方程式_________________。
(6)有机物M是C的一种同分异构体,满足下列条件的同分异构体有___种;其中核磁共振氢谱有4组峰,峰面积之比为2:2:2:1的结构简式为____________。
①苯环上有3个取代基 ②能发生银镜反应
③不能与FeCl3发生显色反应 ④能发生水解反应,且1 mol M消耗4 mol NaOH
(7)设计由苯甲醇为原料制备化合物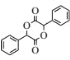 的合成路线______(无机试剂任选)。
的合成路线______(无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个体积为2L的真空密闭容器中加入0.5molCaCO3,发生反应CaCO3(s)![]() CaO (s)+CO2(g),测得二氧化碳的物质的量浓度随温度的变化关系如下图所示,图中A表示CO2的平衡浓度与温度的关系曲线,B表示不同温度下反应经过相同时间时CO2的物质的量浓度的变化曲线。请按要求回答下列问题:
CaO (s)+CO2(g),测得二氧化碳的物质的量浓度随温度的变化关系如下图所示,图中A表示CO2的平衡浓度与温度的关系曲线,B表示不同温度下反应经过相同时间时CO2的物质的量浓度的变化曲线。请按要求回答下列问题:
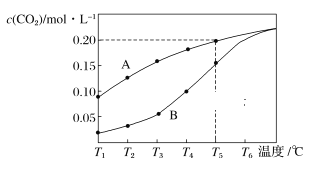
(1)该反应正反应为______(填“吸”或“放”)热反应,温度为T5℃时,该反应耗时40s达到平衡,则T5℃时,该反应的平衡常数数值为________。
(2)如果该反应的平衡常数K值变大,该反应________(选填字母)。
a.一定向逆反应方向移动
b.在平衡移动时正反应速率先增大后减小
c.一定向正反应方向移动
d.在平衡移动时逆反应速率先减小后增大
(3)保持温度、体积不变,充入CO2气体,则CaCO3的质量______,CaO的质量______CO2的浓度________(填“增大”,“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式的书写正确的是( )
A.向Na2S2O3溶液中通入足量氯气:S2O![]() +4Cl2+5H2O=2SO
+4Cl2+5H2O=2SO![]() +8Cl-+10H+
+8Cl-+10H+
B.向AlCl3溶液中加入足量氨水:Al3++4NH3·H2O=AlO![]() +4NH
+4NH![]() +2H2O
+2H2O
C.向碳酸氢铵溶液中加入足量石灰水:Ca2++HCO![]() +OH-=CaCO3↓+H2O
+OH-=CaCO3↓+H2O
D.在海带灰的浸出液(含有I-)中滴加H2O2得到I2:2I-+H2O2+2H+=I2+O2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知C(s、金刚石)+O2(g)![]() CO2(g);ΔH=-395.4 kJ·mol-1,C(s、石墨)+O2(g)
CO2(g);ΔH=-395.4 kJ·mol-1,C(s、石墨)+O2(g)![]() CO2(g);ΔH=-393.5 kJ·mol-1。
CO2(g);ΔH=-393.5 kJ·mol-1。
①石墨和金刚石相比,石墨的稳定性_________金刚石的稳定性。
②石墨中C-C键键能________金刚石中C-C键键能。(均填“大于” “小于”或“等于”)。
(2)将4g CH4完全燃烧生成气态CO2和液态水,放出热量222.5 kJ,其热化学反应方程式为:______________________________________________________。
(3)0.5mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5kJ热量,其热化学反应方程式为:______________________________________________。
(4)已知下列反应的反应热:
CH4(g)+H2O(g)![]() CO(g)+3H2(g) △H1=+206.2kJ·mol-1
CO(g)+3H2(g) △H1=+206.2kJ·mol-1
CH4(g)+CO2(g)![]() 2CO(g)+2H2(g) △H2=-247.4 kJ·mol-1
2CO(g)+2H2(g) △H2=-247.4 kJ·mol-1
则CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是实验室对煤进行干馏的装置图,回答下列问题:
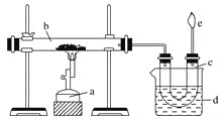
(1)指出图中仪器名称:c______,d______。
(2)仪器d的作用是______,c中液体有______和______,其中无机物里溶有_____,可用_____检验出来。有机物可以通过______的方法使其中的重要成分分离出来。
(3)e处点燃的气体的主要成分有_______,火焰的颜色为_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com