
| A.任何能使熵值减小的过程都能自发进行 |
| B.1mol NaOH分别和1mol CH3COOH、1molHNO3反应,后者比前者△H小 |
C.已知热化学方程式2SO2(g)+O2(g) 2SO3(g);△H=-Q kJ·mol-1(Q>0),则将2mol SO2(g)和1 mol O2(g)置于一密闭容器中充分反应后放出Q kJ的热量 2SO3(g);△H=-Q kJ·mol-1(Q>0),则将2mol SO2(g)和1 mol O2(g)置于一密闭容器中充分反应后放出Q kJ的热量 |
| D.在Na2SO4溶液中加入过量的BaCl2后,溶液中不存在SO42- |
科目:高中化学 来源:不详 题型:单选题
| A.石墨比金刚石稳定 |
| B.金刚石比石墨稳定 |
| C.相同物质的量的石墨比金刚石的总能量高 |
| D.两者互为同位素 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.①②③ | B.②③ | C.①② | D.①③ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 O2(g)===ZnO(s) ΔH1=-Q1 kJ/mol①
O2(g)===ZnO(s) ΔH1=-Q1 kJ/mol① O2(g)===HgO(s) ΔH2=-Q2 kJ/mol②
O2(g)===HgO(s) ΔH2=-Q2 kJ/mol②查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①② | B.②③ | C.①③ | D.①④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.C + CO2=2CO | B.C + O2=CO2 |
| C.2C + O2= 2CO | D.C + CuO=CO2 + Cu |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
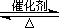 2SO3(g) ?H="-196.6" kJ·mol-1
2SO3(g) ?H="-196.6" kJ·mol-1 2NO2(g) ?H="-113.0" kJ·mol-1
2NO2(g) ?H="-113.0" kJ·mol-1  SO3(g)+NO(g)的?H= kJ·mol-1。
SO3(g)+NO(g)的?H= kJ·mol-1。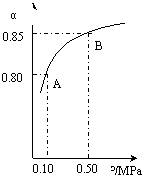
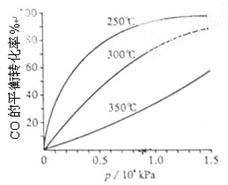
 CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如上图(右)所示。该反应?H 0(填“>”或“ <”)。
CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如上图(右)所示。该反应?H 0(填“>”或“ <”)。 查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.铝热反应 | B.铝与盐酸反应 |
| C.Ba(OH)2·8H2O晶体和NH4Cl晶体反应 | D.灼热的炭与CO2反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com