
【题目】下列有关电池的叙述正确的是
A. 华为 Mate 系列手机采用的超大容量高密度电池是一种一次电池
B. 原电池中的电极一定要由两种不同的金属组成
C. 原电池中发生氧化反应的电极是负极
D. 太阳能电池主要材料为二氧化硅
科目:高中化学 来源: 题型:
【题目】SO2的烟气会形成酸雨,危害环境.利用钠碱循环法可脱除烟气中的SO2 . 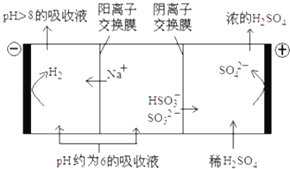
(1)在钠碱循环法中,Na2SO3溶液作为吸收液,可由NaOH溶液吸收SO2制得,该反应的离子方程式是 .
(2)吸收液吸收SO2的过程中,pH随n(SO32﹣),n(HSO3﹣)变化关系如下表:
n(SO32﹣):,n(HSO3﹣) | 91:9 | 1:1 | 1:91 |
PH | 8.2 | 7.2 | 6.2 |
1表判断NaHSO3溶液显性,用化学平衡原理解释:
②当吸收液呈中性时,溶液中离子浓度关系正确的是(选填字母):
a.c(Na﹣)=2c(SO ![]() )+c(HSO
)+c(HSO ![]() )
)
b.c(Na﹣)>c(HSO ![]() )>c(SO
)>c(SO ![]() )>c(H﹣)=c(OH﹣)
)>c(H﹣)=c(OH﹣)
c.c(Na+)+c(H+)=c(SO ![]() )+c(HSO
)+c(HSO ![]() )+c(OH﹣)
)+c(OH﹣)
(3)当吸收液的pH降至约为6时,送至电解槽再生.再生示意图如下:
①HSO3﹣在阳极放电的电极反应式是 .
②当阴极室中溶液PH升至8以上时,吸收液再生并循环利用.简述再生原理: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,某气态平衡体系的平衡常数表达式为K= ![]() ,有关该平衡体系的说法正确的是( )
,有关该平衡体系的说法正确的是( )
A.升高温度,平衡常数K一定增大
B.增大A浓度,平衡向正反应方向移动
C.增大压强,C体积分数增加
D.升高温度,若B的百分含量减少,则正反应是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,下列各组离子能大量共存的是( )
A.稀硫酸中:K+、Mg2+、AlO2﹣、S2O32﹣
B.NaHS溶液中:SO42﹣、K+、Cl﹣、Cu2+
C.![]() =10﹣13mol?L﹣1溶液中:Fe3+、NH4+、Mg2+、SO42﹣
=10﹣13mol?L﹣1溶液中:Fe3+、NH4+、Mg2+、SO42﹣
D.通入大量CO2的溶液中:Na+、ClO﹣、CH3COO﹣、HCO3﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据实验数据,写出下列反应的热化学方程式.
(1)1mol H2(g)与适量O2(g)反应,生成H2O(1),放出285.8kJ热量. .
(2)1mol C2H5OH(1)与适量O2(g)反应,生成CO2(g)和H2O(1),放出1366.8kJ热量. .
(3)2mol Al(s)与适量O2(g)发生反应,生成Al2O3(s),放出1669.8kJ热量. .
(4)已知2.00g C2H2气体完全燃烧生成液态水和CO2 , 放出99.6kJ的热量,写出表示C2H2燃烧热的热化学方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】往含0.2mol NaOH和0.1mol Ba(OH)2的溶液中持续稳定地通入CO2气体,当通入气体的体积为6.72L(标准状况下)时立即停止,则在这一过程中,溶液中离子数目和通入CO2气体的体积关系正确的图象是(气体的溶解忽略不计)( )
A.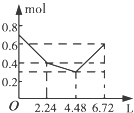
B.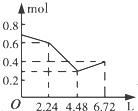
C.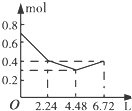
D.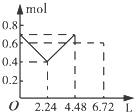
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将标准状况下672mLO2和NH3的混合气体通过灼热的三氧化二铬(催化剂),氨全部被氧化。将反应后气体全部通入水中,无气体剩余,制得100mL溶液,则该溶液的浓度为
A. 1.0mol/L B. 0.1mol/L C. 0.3mol/L D. 3.0mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2015年诺贝尔生理学或医学奖的一半授予我国药物化学家屠吆吆,以表彰她发明抗疟疾新药青蒿素和双氢青蒿素.以异胡薄荷醇为起始原料是人工全合成青蒿素的途径之一(如图).下列说法正确的是( ) 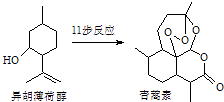
A.异胡薄荷醇的分子式为C10H17O
B.异胡薄荷醇在NaOH醇溶液中可发生消去反应
C.青蒿素分子中含有7个手性碳原子
D.青蒿素在热的酸、碱溶液中均可稳定存在
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com