
| A.原子核都是由质子和中子构成? |
| B.质子数相同的粒子其化学性质不一定相同? |
| C.某种粒子最外层上有8个电子,则一定是稀有气体元素的原子? |
D.原子电子构型为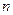 s2 s2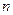 p6的为稀有气体元素? p6的为稀有气体元素? |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:单选题
| 9 | 10 | 11 | |||||||||||||||||||||||||||
| 17 | 18 | 19
查看答案和解析>> 科目:高中化学 来源:不详 题型:填空题 (12分)根据元素周期表的结构,回答下面两个小题。 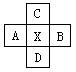 (1)A、B、C、D、X五种元素在周期表中的位置如右图所示(X与A、B为相邻族,与C、D为相邻周期),若元素X的原子序数为x,则A、B、C、D四种元素的原子序数之和为 或 (用含x的代数式表示)。 (2)在下列各元素组中,除一种元素外,其余都可以按照某种共性归属一类,请选出各组的例外元素,并将该组其他元素的可能归属按所给六种类型的编号填入表内。
查看答案和解析>> 科目:高中化学 来源:不详 题型:单选题 用NA表示阿伏加德罗常数,下列说法正确的是
查看答案和解析>> 科目:高中化学 来源:不详 题型:填空题 (本小题15分)A、B、C、D四元素的核电荷数依次增加,它们的离子的电子层数相同且最外层电子数均为8。A原子的L层电子数与K、M层电子数之和相等,D原子的K、L层电子数之和等于电子总数的一半。回答以下问题: (1)四元素的符号依次是A______;B______;C________;D______。 (2)写出B、D元素的离子结构示意图: B.______________________; D.______________________。 (3)用电子式表示A、C元素形成的离子化合物的过程: ________________________________________________________。 (4)在A、B、C、D最高价氧化物水化物中: 比较其中酸的酸性强弱:____________________________; 比较其中碱的碱性强弱:____________________________。 查看答案和解析>> 科目:高中化学 来源:不详 题型:单选题 下列元素一定是主族元素的是( )
查看答案和解析>> 科目:高中化学 来源:不详 题型:单选题 A元素原子的最外层电子数是a,次外层电子数是b;B元素原子的M层电子数是(a-b),L层电子数是(a+b)。则A、B 2种元素形成的化学式可能表示为( ) A.B3A2 B.BA2 C.A3B2 D.AB2 查看答案和解析>> 科目:高中化学 来源:不详 题型:实验题 A、B、C、D四种元素都是短周期元素,A元素的离子具有黄色的焰色反应。B元素的离子结构和Ne具有相同的电子层排布;5.8 g B的氢氧化物恰好能与100 mL 2 mol·L-1盐酸完全反应;B原子核中质子数和中子数相等。H2在C单质中燃烧产生苍白色火焰。D元素原子的电子层结构中,最外层电子数是次外层电子数的3倍。根据上述条件完成下列问题: (1)元素C位于第________周期第________族,它的最高价氧化物的化学式为________。 (2)A元素是________,B元素是________,D元素是________。 (3)A与D形成稳定化合物的化学式是________,该化合物中存在化学键类型为________,判断该化合物在空气中是否变质的简单方法是 ________________________________________。 (4)C元素的单质有毒,可用A的最高价氧化物对应的水化物的溶液吸收,其离子方程式为______________________________________________________________________________。 查看答案和解析>> 同步练习册答案 湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区 违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com版权声明:本站所有文章,图片来源于网络,著作权及版权归原作者所有,转载无意侵犯版权,如有侵权,请作者速来函告知,我们将尽快处理,联系qq:3310059649。 ICP备案序号: 沪ICP备07509807号-10 鄂公网安备42018502000812号 |