
| 检测次数 | 溶液中检测出的物质 |
| 第一次 | KCl、K2SO4、Na2CO3、NaCl |
| 第二次 | KCl、BaCl2、Na2SO4、K2CO3 |
| 第三次 | Na2SO4、KCl、K2CO3、NaCl |
科目:高中化学 来源:不详 题型:单选题
| A.用HF溶液可以除去硅晶体中含有的少量二氧化硅晶体 |
| B.向两份Fe3O4固体中分别加入HCl溶液与HI溶液,二者反应现象一样 |
| C.向某溶液中滴加NaOH溶液后又加入酚酞,溶液呈红色,说明原溶液中含有NH4+ |
| D.向某溶液中加入足量的稀HNO3溶液,所得气体能使澄清石灰水变浑浊,证明该溶液中存在CO32-或HCO3- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氨水 | B.AgNO3 | C.NaOH | D.BaCl2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| | 熔点/℃ | 沸点/℃ | 密度/g·mL-1 | 其他 |
| 黄磷 | 44.1 | 280.5 | 1.82 | 2P(过量)+3Cl2 2PCl3;2P+5Cl2 2PCl3;2P+5Cl2 2PCl5 2PCl5 |
| PCl3 | —112 | 75.5 | 1.574 | 遇水生成H3PO3和HCl,遇O2生成POCl3 |
| POCl3 | 2 | 105.3 | 1.675 | 遇水生成H3PO4和HCl,能溶于PCl3 |
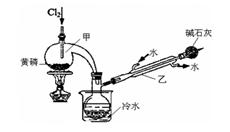
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题



查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
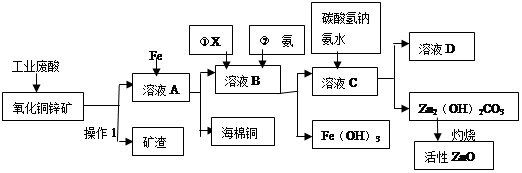
| A.KMnO4 | B.O2 | C.H2O2 | D.NaOH |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
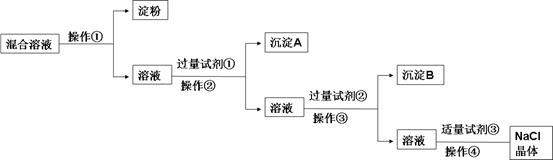
| 编号 | 实验操作 | 预期现象和结论 |
| ① | | |
| ② | | |
| | | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
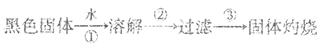
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com