
| A.6g | B.8g | C.10g | D.12g |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:单选题
| A.①②④⑤⑥⑦⑧ | B.②⑤⑥⑦⑨ | C.②④⑤⑥⑦⑧ | D.③④⑤⑥⑦⑧ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.3mol/L的HCl | B.4mol/L的HNO3 |
| C.8mol/L的NaOH | D.18mol/L的H2SO4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
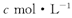 的氢氧化钠溶液V mL,使金属离子刚好沉淀完全,得到的沉淀质量为n g。再将所得沉淀灼烧至质量不再改变为止,得到固体p g0则下列关系不正确的是
的氢氧化钠溶液V mL,使金属离子刚好沉淀完全,得到的沉淀质量为n g。再将所得沉淀灼烧至质量不再改变为止,得到固体p g0则下列关系不正确的是A.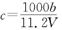 | B.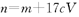 | C. | D. |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.镁原子最外电子层上有2个电子,铝原子最外电子层上有3个电子 |
| B.Mg(OH)2呈碱性,而Al(OH)3呈两性 |
| C.镁的熔沸点低于铝的熔沸点 |
| D.镁的硬度不如铝 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①②③ | B.②③④ | C.①③⑥ | D.②⑤⑥? |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
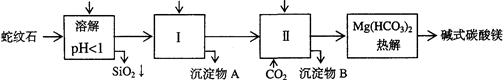
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 1.5 | 3.3 | 9.4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com