
【题目】下图是元素周期表的一部分,表中所列字母分别代表一种元素。
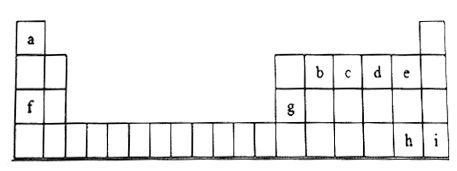
根据表格所给信息,回答下列问题:
(1)c元素原子的最高价氧化物对应的水化物的化学式___________(填化学式)
(2)b、c、d、e的原子半径依次_______(填“增大”或“减小”)
(3)e、h元素原子形成的氢化物中,热稳定性大的是__________(填氢化物的化学式)
(4)f、g元素的最高价氧化物对应水化物之间发生反应的化学方程式__________________
【答案】 HNO3 减少 HF NaOH+Al(OH)3 =Na [Al(OH)4]
【解析】由元素在周期表中位置可知,a为H、b为C、c为N、d为O、e为F、f为Na、g为Al、h为Br,i为Kr。
(1)c的最高价氧化物对应的水化物为硝酸,化学式为HNO3,故答案为:HNO3;
(2)同周期从左向右原子半径减小,则b、c、d、e的原子半径依次减小,故答案为:减小;
(3)非金属性越强,对应氢化物越稳定,则HF更稳定,故答案为:HF;
(4)f、g的最高价氧化物对应水化物分别为氢氧化钠和氢氧化铝,二者反应的化学方程式为NaOH+Al(OH)3 =Na [Al(OH)4]或Al(OH)3 + 2NaOH=NaAlO2 + 2H2O,故答案为:NaOH+Al(OH)3 =Na [Al(OH)4]或Al(OH)3 + 2NaOH=NaAlO2 + 2H2O。


科目:高中化学 来源: 题型:
【题目】已知:![]() ,下列有机物能够合成
,下列有机物能够合成![]() 的组合是( )
的组合是( )
①1,3-丁二烯 ②2-甲基-l,3-丁二烯 ③1,3-戊二烯 ④2,3-二甲基-l,3-丁二烯
⑤2,3-二甲基-l,3-戊二烯 ⑥乙炔 ⑦丙炔 ⑧2-丁炔
A. ①、⑦及④、⑧ B. ⑤、⑥及③、⑧
C. ①、③及②、⑧ D. ②、⑧及④、⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成药物异搏定路线中某一步骤如下:

X Y Z
下列说法不正确的是( )
A. 物质X中所有碳原子可能共平面
B. 可用FeCl3溶液鉴别Z中是否含有X
C. 等物质的量的X、Z分别与H2加成,最多消耗H2的物质的量之比为3∶5
D. 等物质的量的Y、Z分别与NaOH溶液反应,最多消耗NaOH的物质的量之比为1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氨的叙述中,错误的是( )
A. 氨易液化,因此可用作制冷剂
B. 氨易溶解于水,因此可用来做喷泉实验
C. 氨极易溶解于水,因此氨水比较稳定(不容易分解)
D. 氨溶解于水显弱碱性,因此可使酚酞试剂变为红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物Z具有较广泛的抗菌作用,其生成机理可由X与Y相互作用:

下列有关叙述中不正确的是( )
A. Z结构中有4个手性碳原子
B. Y的分子式为C9H8O3
C. 1 mol Z与足量NaOH溶液反应,最多消耗8 mol NaOH
D. Z与浓溴水既能发生取代反应又能发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮元素可以形成许多化合物,在我们生活生产中有广泛的应用。
(1)与NF3分子互为等电子体的分子为________。
(2)铁和氨气在640℃可发生置换反应,产物之一的晶胞结构见图甲。
写出Fe3+的基态电子排布式________。
写出该反应的化学方程式:______________。

(3)维生素B4结构如图乙,则1mol维生素B4分子中含有σ键的数目为______mol。
(4)配合物丙的结构见图,丙中含有__________(填序号);
a.极性共价键 b.非极性共价键 c.配位键 d.氢键
丙中碳原子的杂化方式有______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水氯化铝常作为有机合成和石油化工的催化剂,并用于处理润滑油等。工业上可由金属铝和纯净的氯气作用制备。某课外兴趣小组在实验室里,通过下图所示装置,制取少量纯净的无水氯化铝。据此回答下列问题:
查阅资料:常温下,无水氯化铝为白色晶体,易吸收水分,在178℃升华。装有无水氯化铝的试剂瓶久置潮湿空气中,会自动爆炸并产生大量白雾。

(1)写出A装置中,实验室制取Cl2的离子方程式________________。
(2)仪器甲______(写名称);仪器乙________(写名称)
(3)在E处可收集到纯净的氯化铝,F装置所起的作用是__________。
(4)装置B、C中的试剂分別是_________________。
(5)从A装置中导出的气体若不经过B、C装置而直接进入D装置中,产生的后果是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对有关实验描述和解释正确的是
A. SO2气体通入酸性高锰酸钾溶液中,使高锰酸钾褪色说明SO2有漂白性
B. 浓硝酸在光照条件下变黄,说明浓硝酸易分解生成有色产物且溶于浓硝酸
C. 常温下,将铝、铁片放入浓硫酸、浓硝酸中,无明显现象,说明铝、铁不与冷的浓硫酸、浓硝酸反应
D. 向CuSO4溶液中加入一小块金属钠,则钠与Cu2+反应可置换出铜
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com