
����Ŀ���л���ѧ֪ʶ��������Ӧ�ù㷺��
��1�����ࡢ��֬�͵������Ƕ����Ժ�ֲ����ʳ���еĻ���Ӫ�����ʡ�
�������й�˵���У���ȷ����________________��
A���ޡ��顢ľ�ġ���˿����Ҫ�ɷֶ�����ά��
B����֬�Dz���������ߵ�Ӫ������
C���������������ڷ���ˮ���������ɰ�����
D����������������
E�����ۡ���ά�ء������ʶ�����Ȼ�߷��ӻ�����
F������炙�����Ǧ��Һ���뵽��������Һ�У������ʶ��ܴ���Һ������
��������������Ҫ����ĵ��ǣ�������һ��Ӫ�����ʣ����������ƾ��ȹ�ҵ�ϡ�д�������Ƿ���������Ӧ�Ļ�ѧ����ʽ��_____________________________________________��
��2��ƻ���᳣������ˮ���ǹ������Ӽ�����ṹ��ʽΪ![]() ���÷����й����ŵ�����Ϊ________________�����Ժʹ������ʷ���__________��Ӧ�������Է�����������ˮ���������ᣬ��������ʹ��ˮ��ɫ����������Ľṹ��ʽΪ_________________��
���÷����й����ŵ�����Ϊ________________�����Ժʹ������ʷ���__________��Ӧ�������Է�����������ˮ���������ᣬ��������ʹ��ˮ��ɫ����������Ľṹ��ʽΪ_________________��
��3��ʵ���Һϳ����������IJ������£���Բ����ƿ�ڼ����Ҵ���Ũ��������ᣬƿ����ֱ��װͨ����ȴˮ�������ܣ�ʹ��Ӧ��������������ΪҺ��������ƿ�ڣ������Ȼ���һ��ʱ�������װ�ý�����������ͼ��ʾ�����õ������Ҵ��������ˮ�����������ֲ�Ʒ����ش��������⣺����֪���Ҵ������ᡢ���������ķе�������78.4����118����77.1����
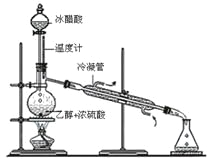
������ƿ�г��˼����Ҵ���Ũ����������⣬��Ӧ���뼸�����Ƭ����Ŀ����_____________��
���������������ķ�Ӧ�ǿ��淴Ӧ����Ӧ�ﲻ����ȫ����������Ӧһ��ʱ��ʹﵽ�˸÷�Ӧ���ȣ����ﵽ��ѧƽ��״̬������������˵���÷�Ӧ�Ѵﵽ��ѧƽ��״̬���У�����ţ�___________________��
A����λʱ�������1mol����������ͬʱ����1molˮ
B����λʱ�������1mol����������ͬʱ����1mol����
C����λʱ�������1mol�Ҵ���ͬʱ����1mol����
D������Ӧ���������淴Ӧ���������
E��������и����ʵ�Ũ�Ȳ��ٱ仯
��������뺬���ᡢ�Ҵ���ˮ�����������ֲ�Ʒ����ͼ�Ƿ��������������ͼ��
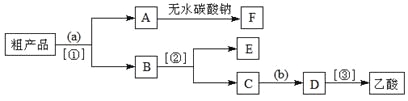
�Լ�a��______�����뷽������_______�����뷽������________���Լ�b��________��
��д��C �� D ��Ӧ�Ļ�ѧ����ʽ________________________________________________��
���𰸡�BCEF CH2OH(CHOH)4CHO + 2Ag(NH3)2OH ![]() 2Ag��+ CH2OH(CHOH)4COONH4+3NH3+ H2O �Ȼ����ǻ� ��������ȡ���� HOOC��CH=CH��COOH ��ֹ��ƿ�е�Һ�屩�� BDE ����Na2CO3��Һ ��Һ ���� ��Ũ������ 2CH3COONa + H2SO4�� 2CH3COOH + Na2SO4
2Ag��+ CH2OH(CHOH)4COONH4+3NH3+ H2O �Ȼ����ǻ� ��������ȡ���� HOOC��CH=CH��COOH ��ֹ��ƿ�е�Һ�屩�� BDE ����Na2CO3��Һ ��Һ ���� ��Ũ������ 2CH3COONa + H2SO4�� 2CH3COOH + Na2SO4
��������
��1����A.�ޡ��顢ľ�ĵ���Ҫ�ɷ�����ά�أ���˿����Ҫ�ɷ��ǵ����ʣ�A����
B.���ࡢ��֬���������У���֬�Dz���������ߵ�Ӫ�����ʣ�B��ȷ��
C.��������������ˮ������ղ����ǰ����ᣬC��ȷ��
D.���������ζ������ۡ���ά�ص�û����ζ��D����
E.���ۡ���ά�ء������ʶ�����Ȼ�߷��ӻ����E��ȷ��
F.����識��뵽��������Һ�У������ʷ�������������Һ������������Ǧ���뵽��������Һ�У������ʷ������Զ�������F��ȷ��
��ѡBCEF��
�������ǵĽṹ��ʽΪCH2OH��CHOH��4CHO����ṹ�к�ȩ��������������Һ����������Ӧ����Ӧ�Ļ�ѧ����ʽΪCH2OH(CHOH)4CHO + 2Ag(NH3)2OH![]() 2Ag��+ CH2OH(CHOH)4COONH4+3NH3+ H2O��
2Ag��+ CH2OH(CHOH)4COONH4+3NH3+ H2O��
��2������ƻ����Ľṹ��ʽ��֪��ƻ�����к��еĹ����ŵ�����Ϊ�ǻ����Ȼ�����Ϊ���Ȼ������Կ��봼�����ʷ���������Ӧ��������ӦҲ��һ��ȡ����Ӧ���ṹ�к��ǻ������ǻ�����̼ԭ�ӵ���̼������Hԭ�ӣ���ƻ���ᷢ����ȥ��Ӧ���������ᣬ��������ʹ��ˮ��ɫ��������Ľṹ��ʽΪHOOC��CH=CH��COOH��
��3���ٶ�Һ���������ʱ��Ϊ��ֹҺ�����ʱ�ľ�����������Ҫ���뼸�����Ƭ�����������Ƭ��Ŀ���ǣ���ֹ��ƿ�е�Һ�屩�С�
��A. ��λʱ�������1mol����������ͬʱ����1molˮ��ֻ��ʾ����Ӧ������˵����Ӧ�ﵽƽ��״̬��
B. ��λʱ�������1mol����������ͬʱ����1mol���ᣬ��ʾ�����淴Ӧ������ȣ���˵����Ӧ�ﵽƽ��״̬��
C. ��λʱ�������1mol�Ҵ���ͬʱ����1mol���ᣬֻ��ʾ����Ӧ������˵����Ӧ�ﵽƽ��״̬��
D. ����Ӧ���������淴Ӧ����������ǿ��淴Ӧ�ﵽƽ��״̬�ı��ʱ�־��
E. ������и����ʵ�Ũ�Ȳ��ٱ仯�ǿ��淴Ӧ�ﵽƽ��״̬��������־��
��ѡBDE��
���������������к����Ҵ��������ˮ�����ȼ�����Լ�aΪ����Na2CO3����Ϊ����Na2CO3��Һ�ܽ��������������ܽ�ȣ������Ҵ�����������ת��Ϊ�����ƣ����뱥��Na2CO3��Һ�������ó��ֲַ����ʷ��뷽����Ϊ��Һ��B��ˮ���к��Ҵ��������ƣ�Ϊ�˽�B�гɷַ�������Ҵ������뷽����Ϊ����EΪ�Ҵ���CΪ��������Һ�����������������ᣬ���ݡ�ǿ�������ᡱ�ĸ��ֽⷴӦ���ɣ���������ӷ�����C�м������ᣬ�����������Ʒ�Ӧ�������ᣬ���D����õ����ᡣ
��C��D�Ļ�ѧ����ʽΪ2CH3COONa+H2SO4��2CH3COOH+Na2SO4��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£���һ��2 L������ܱ�������(Ԥ��װ�����)ͨ��1 mol N2��3 mol H2������һ��ʱ����������ѹǿ����ʼʱ��0.9�����ڴ�ʱ�����H2��ƽ����Ӧ����Ϊ0.1 mol��L��1��min��1����ʱ��Ϊ( ����)
A. 2 minB. 3 minC. 4 minD. 5 min
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���߾���H��һ�ֹ�̽������е�һ�ֺϳ�·�����£�
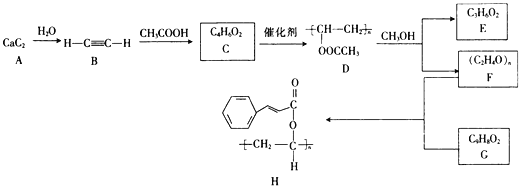
�ش��������⣺
��1��B�Ļ�ѧ������_________��
��2��B����C�ķ�Ӧ����Ϊ_________��F��G��Ӧ����H�ķ�Ӧ����Ϊ_________��
��3��H�й����ŵ�����Ϊ___________________________��
��4��C�Ľṹ��ʽΪ__________________��G�Ľṹ��ʽΪ__________________��
��5����֪E��D��F��CH3OH�ֱ�����ͬ�Ĺ����ţ�д��D��CH3OH��Ӧ����E��F�Ļ�ѧ����ʽ��________��
��6�������廯����X��G��ͬ���칹�壬1 mol X������������Һ��Ӧ����4 mol Ag����X�Ľṹ��ʽ��_____�������������칹���֣�д���˴Ź���������ʾ�����ֲ�ͬ��ѧ�������⣬�ҷ����֮��Ϊ1:2:2:2:1��X�Ľṹ��ʽ��___________����дһ�֣���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʾ��ͼ�뻯ѧ����������ݲ�������ǣ�ˮ����������Ӧ���ӷ��ű�ʾ��
A | B | C | D |
|
|
|
|
NaCl����ˮ | ����������ʴԭ�� | ͭпԭ��ع����ԭ�� | N2��O2��Ӧ�����仯 |
NaCl��Na+ + Cl�� | ������Fe �� 2e����Fe2+ | �ܷ�Ӧ��Zn + Cu2+��Zn2+ + Cu | N2(g) + O2(g)��2NO(g)��H����180 kJ��mol��1 |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ķ���ϩ�������Ժͻ�ѧ�ȶ��Գ����������ϣ�����Ϊ��������������ϳ�·�����£�
���ȼ���![]() ����һ�ȼ���
����һ�ȼ���![]() �ķ���ϩ
�ķ���ϩ![]() ���ķ���ϩ
���ķ���ϩ
����˵���в���ȷ����( )
A.��������������ʹ���Ը��������Һ��ɫ
B.���ȼ���(CHCl3)�����ü�����������ȡ����Ӧ�Ƶ�
C.�ķ���ϩ(CF2��CF2)�����е�ԭ�Ӷ���ͬһƽ����
D.����һ�ȼ���(CHClF2)������ԭ���������Ӷ��ﵽ��8�����ȶ��ṹ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�������£������ܱ������н��еķ�Ӧ��2SO2(g) + O2(g) ![]() 2SO3(g)������˵���ܳ��˵���÷�Ӧ�Ѵﵽ��ѧƽ��״̬����
2SO3(g)������˵���ܳ��˵���÷�Ӧ�Ѵﵽ��ѧƽ��״̬����
A. �����淴Ӧ���ʶ������� B. SO2��O2��SO3��Ũ�����
C. SO2��O2��SO3�������й��� D. SO2��O2��SO3��Ũ�Ⱦ����ٱ仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʹ������ʵ��װ�ý�����Ӧ��ʵ�飬�ܴﵽʵ��Ŀ�ĵ��ǣ� ��
A.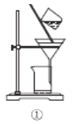 ʹ��װ�âٷ��뱽���屽�Ļ����Һ
ʹ��װ�âٷ��뱽���屽�Ļ����Һ
B.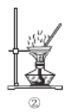 ʹ��װ�â�ֱ�Ӵ�MgCl2��Һ�нᾧ�õ�MgCl2����
ʹ��װ�â�ֱ�Ӵ�MgCl2��Һ�нᾧ�õ�MgCl2����
C.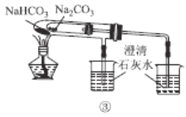 ʹ��װ�â۱Ƚ�Na2CO3��NaHCO3���ȶ���
ʹ��װ�â۱Ƚ�Na2CO3��NaHCO3���ȶ���
D.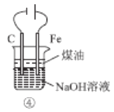 ʹ��װ�â��Ʊ�������ɫ��Fe(OH)2
ʹ��װ�â��Ʊ�������ɫ��Fe(OH)2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����к͵ζ����ⶨij�ռ���Ʒ�Ĵ��ȣ���ش��������⣺
��1��ȷ����5.0 g���������������ʵ���Ʒ�����ʲ������ᷴӦ�������250 mL������Һ���õ��IJ����������ձ�������������ͷ�ιܡ�___________________��
��2���ζ�ʱ����0.2000 mol��L��1���������ζ�������Һ����ȡ����Һ10.00 mLӦѡ��_________����(����ĸ)��
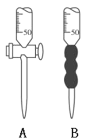
��3���ζ������У��۾�Ӧע��___________________________________���Լ�����ָʾ������ȷ�жϵζ��յ��������________________________________��
��4�����±���֪����2�����������������ƫ������ܵ�ԭ����_________��
�ζ����� | ������Һ���(mL) | ������� | |
�ζ�ǰ�Ŀ̶�(mL) | �ζ���Ŀ̶�(mL) | ||
��һ�� | 10.00 | 0.40 | 20.50 |
�ڶ��� | 10.00 | 2.10 | 24.20 |
������ | 10.00 | 4.10 | 24.00 |
a����ƿ�ô���Һ��ϴ
b���ζ���������ƿ����Һ����ƿ��
c���ζ�ǰ�ζ��ܼ��������ݣ��ζ�����������ʧ
d���ζ�����ʱ�����Ӷ���
��5�����ݱ������ݣ����㱻���ռ���Һ�����ʵ���Ũ����_________���ռ���Ʒ�Ĵ�����_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������軯�أ�K4[Fe(CN)6])˫�ƻ�Ѫ�Σ���һ����Ҫ�Ļ���ԭ�ϡ����������������ķ�ӦΪ��K4[Fe(CN)6]+FeCl3=KFe[Fe(CN)6]��(������) +3KCl���ش����⣺
(1)д����̬Fe3+�ĺ�������Ų�ʽ_________��
(2)K4[Fe(CN)6]�е������������ۼ��⣬����______��________������12mol ������K4[Fe(CN)6�����ʵ���Ϊ________mol��
(3)��Ѫ����Nԭ�ӵ��ӻ���ʽΪ______��C��N��O�ĵ�һ�������ɴ�С������Ϊ_____���縺���ɴ�С������Ϊ________��
(4)Fe��Na��K�ľ���ṹ��ͼ��ʾ��
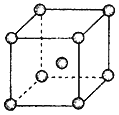
�� �Ƶ��۵�ȼظ��ߣ�ԭ����__________________________��
�� Feԭ�Ӱ뾶��r cm�������ӵ�����ΪNA���������ԭ������Ϊa���������ʵ��ܶ���_______g/cm3��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com