
| A. | 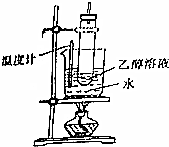 除去酒精中的水 | B. |  验证乙醇的氧化性 | ||
| C. | 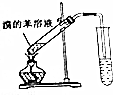 制备溴苯 | D. | 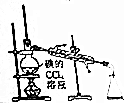 分离CCl4和碘单质 |
分析 A.水浴加热不能除去乙醇中的水,直接蒸馏乙醇与水易形成共沸混合物;
B.Cu氧化生成CuO,CuO氧化乙醇生成乙醛;
C.制备溴苯需要催化剂;
D.CCl4和碘单质互溶,但沸点不同.
解答 解:A.水浴加热不能除去乙醇中的水,直接蒸馏乙醇与水易形成共沸混合物,应加CaO、蒸馏除去乙醇中的水,故A错误;
B.Cu氧化生成CuO,CuO氧化乙醇生成乙醛,则实验可验证乙醇的还原性,故B错误;
C.制备溴苯需要催化剂,利用苯、液溴、铁粉制备溴苯,故C错误;
D.CCl4和碘单质互溶,但沸点不同,图中温度计的位置、冷水方向均合理,故D正确;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握混合物分离提纯、物质制备实验、性质实验及实验装置的作用为解答的关键,侧重分析与实验能力的考查,注意实验评价性分析,题目难度不大.


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
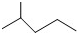 表示的分子式是C6H14;名称是2-甲基戊烷.
表示的分子式是C6H14;名称是2-甲基戊烷.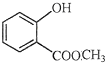 中含有的官能团的名称为羟基、酯基.
中含有的官能团的名称为羟基、酯基.查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙酸分子中含有的官能团是羧基(-COOH) | |
| B. | 乙酸俗称酒精 | |
| C. | 乙酸与苏打(碳酸钠)作用会有气泡产生 | |
| D. | 在发生酯化反应时,乙酸分子中的羟基跟醇分子中羟基上的氢原子结合成水分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 X、Y、Z、R、M是原子序数依次增大的五种元素,基态X原子的2p电子数是2s电子数的一半,由Y、Z元素合物是一种常用的漂白剂、供氧剂,Z和R位于同周期且R的基态原子中有3个电子能量最高,M2+与过量氨水作用先得到蓝色沉淀后转化为深蓝色溶液Q,请回答下列问题:
X、Y、Z、R、M是原子序数依次增大的五种元素,基态X原子的2p电子数是2s电子数的一半,由Y、Z元素合物是一种常用的漂白剂、供氧剂,Z和R位于同周期且R的基态原子中有3个电子能量最高,M2+与过量氨水作用先得到蓝色沉淀后转化为深蓝色溶液Q,请回答下列问题:查看答案和解析>>
科目:高中化学 来源:2017届福建省高三上第二次月考化学试卷(解析版) 题型:选择题
有100 mL 3.5 mol·L-1的NaOH溶液和100 mL 1 mol/L的AlCl3溶液,按如下两种方法进行实验:
①将NaOH溶液分多次加入到AlCl3溶液中(边加边搅拌);
②将AlCl3溶液分多次加入到NaOH溶液中(边加边搅拌)。
比较两次实验的结果,其中正确的是( )
A.现象相同,沉淀量相等 B.现象不同,沉淀量不等
C.现象相同,沉淀量不等 D.现象不同,沉淀量相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com