
下列有关钢铁腐蚀与防护的说法正确的是( )
A.钢管与电源正极连接,钢管可被保护
B.铁遇冷浓硝酸表面钝化,可保护内部不被腐蚀
C.钢管 与铜管露天堆放在一起时,钢管不易被腐蚀
与铜管露天堆放在一起时,钢管不易被腐蚀
D.钢铁发生析氢腐蚀时,负极反应是Fe-3e-===Fe3+
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
Na2FeO4是一种高效多功能水处理剂,应用前景十分看好。一种制备Na2FeO4的方法可用化学方程式表示如下:2FeSO4 + 6Na2O2 = 2Na2FeO4 + 2Na2O + 2Na2SO4 + O2↑,对此反应下列说法中正确的是
A.Na2O2只作氧化剂 B.FeSO4只作还原剂
C.铁元素被还原
D.2 mol FeSO4发生反应时,反应中共有8 mol电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
Fe2+和Fe3+可以互相转化,现提供的物质有FeCl2溶液、FeCl3溶液、Fe粉、
KSCN溶液、3%H2O2,请你完成实验报告证明Fe2+和Fe3+的互相转化。
| 实 验 步 骤 | 实 验 现 象 | 结 论 |
| 1.①将KSCN溶液滴入盛有FeCl2溶液的试管中,充分振荡 ②再滴入______________,充分振荡 | ①__________________ ②溶液变红 | Fe2+被Cl2氧化成 Fe3+ |
| 2.①在盛有足量Fe粉的试管中滴入FeCl3溶液,充分振荡 ②再滴入KSCN溶液,充分振荡 | ①溶液由___________色变为___________色 ②无明显现象 | __________________________ |
查看答案和解析>>
科目:高中化学 来源: 题型:
如图装置Ⅰ是一种可充电电池,装置Ⅱ为电解池。装置Ⅰ的离子交换膜只允许Na+通过,已知电池充放电的化学方程式为:2Na2S2+NaBr3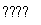 Na2S4+3NaBr,当闭合开关K时,X电极附近溶液变红。下列说法正确的是 ( )。
Na2S4+3NaBr,当闭合开关K时,X电极附近溶液变红。下列说法正确的是 ( )。
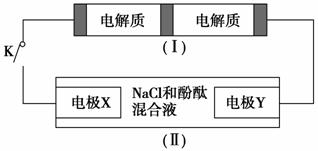
A.闭合开关K时,钠离子从右到左通过离子交换膜
B.闭合开关K时,负极反应式为:3NaBr-2e-===NaBr3+2Na+
C.闭合开关K时,X电极反应式为:2Cl--2e-===Cl2↑
D.闭合开关K时,当有0.1 mol Na+通过离子交换膜时,X电极上放出标准状
况下气体1.12 L
查看答案和解析>>
科目:高中化学 来源: 题型:
铝及铝合金经过阳极氧化,铝表面能生成几十微米厚的 氧化铝膜。某研究性学习小组模拟工业法对铝片表面进行氧化处理。分别以铅片、铝片为电极,以硫酸溶液为电解液,按照如图所示装置连接电解池装置,电解40 min后取出铝片,用水冲洗,放在水蒸气中封闭处理20~30 min,即可得到更加致密的氧化膜。下列有关说法正确的是 ( )。
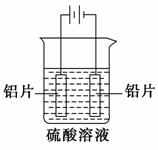
A.电解时电子从电源负极→导线→铝极,铅极→导线→电源正级
B.在电解过程中,H+向阳极移动,SO42-向阴极移动
C.电解过程阳极周围溶液的pH下降
D.电解的总反应为2Al+6H+===2Al3++3H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
向2 L密闭容器中通入6mol气体A和6mol气体B,在一定条件下发生反应:
xA(g)+yB(g)=pC(g)+qD(g) 已知:平均反应速率v(C)=1/2v(A);反应2 min时,A的浓度减少了1mol/L,B的物质的量减少了3mol,有6mol D生成。回答下列问题:
(1)反应2 min内,v(A)= ,v(B)= ;
(2)该反应化学方程式中x:y:p:q= ;
(3)如果其他条件不变,将容器的容积变为1 L,进行同样的实验,则与上述反应比较:反应速率 (填“增大”、“减小”或“不变”),理由是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com