
在光照的条件下,将1 mol甲烷与一定量的氯气充分混合,经过一段时间,甲烷和氯气均无剩余,生成一氯甲烷、二氯甲烷、三氯甲烷、四氯化碳和氯化氢,若已知生成的二氯甲烷、三氯甲烷、四氯化碳的物质的量分别为a mol,b mol,c mol,该反应中消耗的氯气的物质的量是( )
A.(1-a-b-c)mol B.(1+a+2b+3c) mol
C.(2a+3b+4c)mol D.(a+b+c)mol
 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源:2015-2016学年新疆农业大学附中高一下学期期中化学试卷(解析版) 题型:选择题
在一定温度下的定容密闭容器中,发生反应:A(g)+2B(g)  3C(g)。当下列物理量不再变化时,不能表明反应已达平衡的是 ( )
3C(g)。当下列物理量不再变化时,不能表明反应已达平衡的是 ( )
A.混合气体的压强 B.A的浓度不再变化 C.正逆反应速率相等 D.C的质量不再变化
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二下期末化学试卷(解析版) 题型:填空题
卤族元素的单质和化合物很多我们可以利用所学物质结构与性质的相关知识去认识和理解它们。
(1)卤族元素位于周期表的________区;溴的价电子排布式为________;
(2)请根据如表提供的第一电离能数据判断:最有可能生成较稳定的单核阳离子的卤素原子是________。
| 氟 | 氯 | 溴 | 碘 | 铍 |
第一电离能(kJ/mol) | 1681 | 1251 | 1140 | 1008 | 900 |
(3)已知高碘酸有两种形式,化学式分别为H5IO6(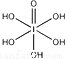 )和HIO4,前者为五元酸,后者为一元酸.请比较二者酸性强弱:H5IO6________ HIO4.(填“>”、“<”或“=”)
)和HIO4,前者为五元酸,后者为一元酸.请比较二者酸性强弱:H5IO6________ HIO4.(填“>”、“<”或“=”)
(4) 与KI3类似的,还有CsICl2等.已知CsICl2不稳定,受热易分解,倾向于生成晶格能更大的物质,则它按下列________式发生.
A.CsICl2=CsCl+ICl B.CsICl2=CsI+Cl2
(5)已知ClO2-为角型,氯原子的杂化轨道类型为________,与ClO2-互为等电子体的微粒是________。(任写一个)
(6)下图为碘晶体晶胞结构.有关说法中正确的是________
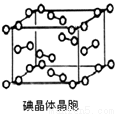
A.碘分子的排列有2种不同的取向,2种取向不同的碘分子以4配位数交替配位形成层结构
B.用均摊法可知平均每个晶胞中有4个碘原子
C.碘晶体为无限延伸的空间结构,是原子晶体
D.碘晶体中存在的相互作用有非极性键和范德华力
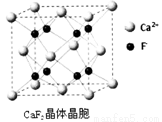
(7)已知CaF2晶体(见图)的密度为ρg/cm3,NA为阿伏加德罗常数,相邻的两个Ca2+的核间距为a cm,则CaF2的相对分子质量可以表示为________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二下期末化学试卷(解析版) 题型:选择题
下列有机物的命名中,正确的是( )
A.4-甲基-4,5-二乙基己烷
B.2,3-二甲基-2,4-戊二烯
C.CH3CH(OH)CH2CH3:丁醇
D.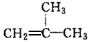 2一甲基-1-丙烯
2一甲基-1-丙烯
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高一下期末化学试卷(解析版) 题型:推断题
表中所列字母分别代表一种元素。
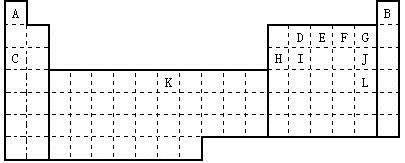
(1)G的气态氢化物比J的气态氢化物 (填“稳定”或“不稳定”,此空1分)。
(2)在一定条件下,A与E可形成一种极易溶于水的气态化合物,其电子式为________;该物质溶于水后的溶液呈________性(填“酸”、“碱”或“中”)。
(3)元素C和H的最高价氧化物对应的水化物相互反应的离子方程式为: 。
(4)元素G和L的原子序数相差: ,它们的氢化物的水溶液酸性相对强的是: (填化学式)
(5)表中A和F两种元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为:
A.MnO2B.Na2SO4C.FeCl3D.KMnO4
(6)K为生产、生活中应用最广泛的金属,通常采用的冶炼方法为:
A.电解法 B.热分解法 C.热还原法
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高一下期末化学试卷(解析版) 题型:选择题
下列烷烃在光照条件下与氯气反应,只生成一种一氯代烃的是 ( )
A.CH3 CH2 CH2CH3
B.(CH3)3C C(CH3)3
C.CH3CH(CH3)CH3
D.CH3C(CH3)2CH2 CH2CH3
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高一下期末化学试卷(解析版) 题型:选择题
在25 ℃,101 kPa下,1 mol的白磷(化学式为P4)完全燃烧放出的热量比4 mol的红磷(化学式为P)完全燃烧放出的热量多。化学方程式分别为P4(s)+5O2(g)===P4O10(s);
4P(s)+5O2(g)===P4O10(s)。由此判断,下列说法正确的是( )
A.由红磷转化为白磷是吸热反应,等质量时红磷能量比白磷高
B.由红磷转化为白磷是吸热反应,等质量时红磷能量比白磷低
C.由红磷转化为白磷是放热反应,等质量时红磷能量比白磷高
D.由红磷转化为白磷是放热反应,等质量时红磷能量比白磷低
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏高二下期末化学试卷(解析版) 题型:选择题
下列说法合理的是
A.液态氟化氢中存在氢键,所以其分子比氯化氢更稳定
B.由水溶液的酸性:HCl>H2S,可推断出元素的非金属性:Cl>S
C.邻羟基苯甲醛沸点高于对羟基苯甲醛是因为形成了分子内氢键
D.若X+和Y2-的核外电子层结构相同,则原子序数: Y<X
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com