
| 80℃,通电 |
| Ⅰ |
| 室温,KCl |
| Ⅱ |
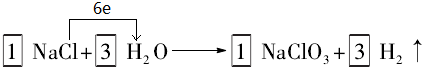 ;
; ;
;

科目:高中化学 来源: 题型:
A、N2+O2
| |||
| B、2NO+O2→2NO2 | |||
| C、3NO2+H2O→2HNO3+NO | |||
D、4NH3+5O2
|
查看答案和解析>>
科目:高中化学 来源: 题型:
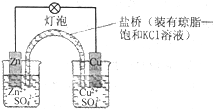
| A、盐桥中的Cl-移向CuSO4溶液 |
| B、电池总反应为Zn+Cu2+=Zn2++Cu |
| C、在外电路中,电子从正极流向负极 |
| D、取下盐桥,原电池仍可工作 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | A | B | C | D |
| n(CO2) mol | 2 | 3 | 4 | 6 |
| n(沉淀) mol | 1 | 2 | 4 | 3 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 mol Cl2与足量NaOH反应,转移的电子数为2nA |
| B、1 mo1Na被完全氧化生成Na2O2,失去的电子数为2nA |
| C、常温常压下,22.4LSO2气体中含有的原子数小于3nA |
| D、0.1 mol/LNaOH溶液中含有Na+的数目为0.1 nA |
查看答案和解析>>
科目:高中化学 来源: 题型:
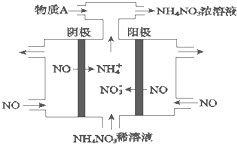 (1)室温下,向Na2S的水溶液中加入等体积等浓度的盐酸,反应后所得的溶液中,除氢离子之外的离子浓度由小到大的顺序为:
(1)室温下,向Na2S的水溶液中加入等体积等浓度的盐酸,反应后所得的溶液中,除氢离子之外的离子浓度由小到大的顺序为:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、酸式滴定管用蒸馏水洗净后,必须用已知浓度的盐酸润洗 |
| B、锥形瓶用蒸馏水洗净后,用NaOH溶液润洗后再加入待测液 |
| C、滴定时,必须逐出滴定管下口的气泡 |
| D、读数时,视线与滴定管内液体的凹液面最低处保持水平 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com