
 SO4��NH4HSO4�����������ɣ��ֳ�ȡ����Ʒ�ķݣ��ֱ������ͬŨ�ȵ�NaOH��Һ��40.00mL��������120�����ң�ʹ����ȫ���ݳ�[(NH4)2SO4��NH4HSO4�ķֽ��¶Ⱦ�����200��]������й�ʵ���������£���״������
SO4��NH4HSO4�����������ɣ��ֳ�ȡ����Ʒ�ķݣ��ֱ������ͬŨ�ȵ�NaOH��Һ��40.00mL��������120�����ң�ʹ����ȫ���ݳ�[(NH4)2SO4��NH4HSO4�ķֽ��¶Ⱦ�����200��]������й�ʵ���������£���״������


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��Ũ���ᡢŨ�����ڼ��������¶��ܽ�ľ̿����Ϊ������̼ |
| B�������������������Ȼ�����Һ�ֱ�������ɲ����գ����յõ������ʳɷֲ�ͬ |
C����NaClO��Һ��ͨ������SO2�����ӷ���ʽ��ClO-��SO2��H2O=HClO��HSO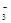 |
| D������������ϡ���ᷴӦʱ���������뻹ԭ�������ʵ���֮��Ϊ2��3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����
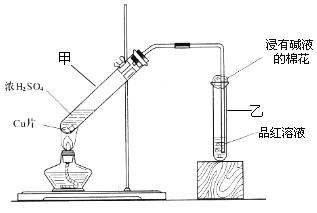
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
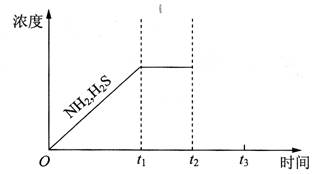
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����
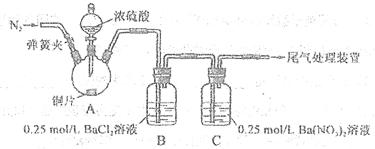
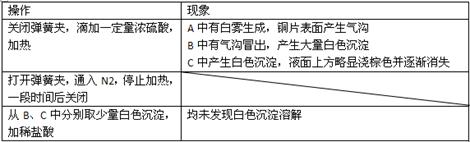
| �� | ������ɫ���� |
| �� | ������ɫ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����

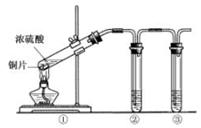
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 �ʣ���ȷ�ķ�����
�ʣ���ȷ�ķ�����| A��ȡ������Ʒ���Թ��У�����ϡ���ᣬ�������ٵ���BaCl2��Һ�����а�ɫ������������˵���ѱ��ʡ� |
| B��ȡ������Ʒ���Թ��У�����ϡ���ᣬ�ٵ���BaCl2��Һ�����а�ɫ������������˵���ѱ��ʡ� |
| C��ȡ������Ʒ���Թ��У�����ϡ���ᣬ�ٵ���BaCl2��Һ�����а�ɫ������������˵���ѱ��ʡ� |
| D��ȡ������Ʒ���Թ��У�����ϡ���ᣬ������ʹƷ����Һ��ɫ�����壬��˵���ѱ��� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com