
| A. | $\frac{m-n-2}{w•m}$mol | B. | $\frac{w(m-n)}{n}$mol | C. | $\frac{w}{n}$(m-n-2)mol | D. | $\frac{w}{m}$(m-n+2)mol |
分析 R原子的质量数为m,则其摩尔质量为mg/mol,根据n=$\frac{m}{M\\;}$计算原子的物质的量;质量数=质子数+中子数,再由阴离子R2-核外有n个中子,则质子数为m-n,阴离子中:质子数+所带电荷数=核外电子数,该离子的核外电子总数为m-n+2,以此解答该题.
解答 解:元素R的质量数为m,其摩尔质量为mg/mol,则Wg R2-阴离子物质的量为:$\frac{wg}{mg/mol}$=$\frac{w}{m}$mol,
离子Rn-核外有n个中子,质量数=质子数+中子数,则质子数为:m-n,阴离子中质子数+所带负电荷数=核外电子数,则Rn-离子的核外电子总数为:m-n+2,
所以Wg Rn-电子的物质的量为:$\frac{w}{m}$mol×(m-n+2)=$\frac{w}{m}$(m-n+2)mol,
故选D.
点评 本题考查学生利用原子构成的简单计算,题目难度不大,明确原子的物质的量的计算是解答本题的关键,注意电子的质量可忽略,质量数近似等于相对原子质量.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
. )为C的同系物,写出符合下列条件的X的一种同分异构体的结构简式:
)为C的同系物,写出符合下列条件的X的一种同分异构体的结构简式: 或
或 或
或 (以上一种即可).
(以上一种即可). ②
② 为原料制备
为原料制备 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
的合成路线流程图(无机试剂任用).合成路线流程图示例如下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 已知反应mA(g)+nB(g)?xC(g)+yD(g),A的转化率RA与p、T的关系如图,根据图示可以得出的正确结论是( )
已知反应mA(g)+nB(g)?xC(g)+yD(g),A的转化率RA与p、T的关系如图,根据图示可以得出的正确结论是( )| A. | 正反应吸热,m+n>x+y | B. | 正反应吸热,m+n<x+y | ||
| C. | 正反应放热,m+n>x+y | D. | 正反应放热,m+n<x+y |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
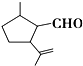 有机物A是一种重要的化工原料,其结构简式如图,下列检验A中官能团的试剂和顺序正确的是( )
有机物A是一种重要的化工原料,其结构简式如图,下列检验A中官能团的试剂和顺序正确的是( )| A. | 先加KMnO4酸性溶液,再加银氨溶液,微热 | |
| B. | 先加溴水,再加KMnO4酸性溶液 | |
| C. | 先加银氨溶液,微热,再加溴水 | |
| D. | 先加入足量的新制Cu(OH)2悬浊液,微热,酸化后再加溴水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{m}{a}$mol | B. | $\frac{2m}{3}$mol | C. | (m+n)mol | D. | $\frac{2(m+n)}{3a}$mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com