
 ���ĺϳ���Ŀǰ�ձ�ʹ�õ��˹��̵�������
���ĺϳ���Ŀǰ�ձ�ʹ�õ��˹��̵����������� ��1������ͼ1�������Ӧ�ȣ�д���Ȼ�ѧ����ʽ��ע������״̬����Ӧ�ȷ��ŵȣ������ܽ��ͷ�Ӧ�Ļ�ܣ�
��2������ƽ��״̬���ж������жϣ�ֻҪ��������Ӧ���ʵ����淴Ӧ���ʣ������жϣ�
��� �⣺��1����ͼ1��֪��1molN2��g����3molH2��g����ȫ��Ӧ����2molNH3��g���ķ�Ӧ��Ϊ508kJ/mol-600kJ/mol=-92kJ/mol��
���Ժϳɰ����Ȼ�ѧ��Ӧ����ʽΪN2��g��+3H2��g��?2NH3��g����H=-92kJ/mol�������ܽ��ͷ�Ӧ�Ļ�ܣ�b��ܽϵͣ�
�ʴ�Ϊ��N2��g��+3H2��g��?2NH3��g����H=-92 kJ•mol-1��b��
��2��A��3�ԣ�H2����=2�ԣ�NH3����˵����v ��NH3������v ��H2�����T3��2�����ڶ�Ӧ��ѧ������֮�ȣ�������Ӧ���ʲ������淴Ӧ���ʣ���A����
B����λʱ��������n mol N2��ͬʱ����2n molNH3˵������Ӧ���ʵ����淴Ӧ���ʣ���B��ȷ��
C��������䣬������������䣬�ܶ�Ҳ��䣬���ܶȲ��������ַ�ƽ��״̬��ƽ��״̬����C����
D����ӦN2��g��+3H2��g��?2NH3��g���Ƿ�Ӧǰ������������ʵ�������ȵķ�Ӧ��������̶�ʱ�����ݰ���٤�����ɿ�֪���¶ȡ������ͬʱ����������ʵ���֮�ȵ���ѹǿ֮�ȣ���������ѹ����ʱ��仯��˵������������ʵ������ٷ����仯����˵�����淴Ӧ�ﵽ�˻�ѧƽ��״̬����D��ȷ��
��ѡB D��
���� ���⿼�����Ȼ�ѧ����ʽ����д��ƽ��״̬���ж����ݺͷ�������Ŀ�ѶȲ���ע�����֪ʶ��Ӧ�ã�


 �����������Ů��ͯ������ϵ�д�
�����������Ů��ͯ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����5%NaCl��Һʱ����������NaCl�����ձ��мӼ�����ˮ�����ܽ� | |
| B�� | ����1mol•L-1NaOH��Һʱ�����ܽ���NaOH��Һ����ע������ƿ | |
| C�� | ����0.1mol/L��H2SO4��Һʱ������ȡ��ŨH2SO4��������ƿ�м�ˮϡ�� | |
| D�� | ȡ��һС����ʱ����ʣ����ƶ�����Һ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| T/�� | 700 | 800 | 900 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ����ͼ��ʯī���缫�ĵ����У�����500mL��һ�����ʵ�ij��ɫ��Һ��pH=4�����е�⣬�۲쵽A�缫�����к�ɫ�Ĺ�̬�������ɣ�B�缫����ɫ�������ɣ�����Һ�е�ԭ��������ȫ����ֹͣ��⣬ȡ��A�缫��ϴ�ӡ�����������缫����1.6g����ش��������⣺
����ͼ��ʯī���缫�ĵ����У�����500mL��һ�����ʵ�ij��ɫ��Һ��pH=4�����е�⣬�۲쵽A�缫�����к�ɫ�Ĺ�̬�������ɣ�B�缫����ɫ�������ɣ�����Һ�е�ԭ��������ȫ����ֹͣ��⣬ȡ��A�缫��ϴ�ӡ�����������缫����1.6g����ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ǽ������ʷ�����һ�������ۼ�����ֻ�зǽ���ԭ�Ӽ�����γɹ��ۼ� | |
| B�� | �ɷǽ���Ԫ����ɵĻ����ﲻһ���ǹ��ۻ����� | |
| C�� | �Ǽ��Լ�ֻ������˫ԭ�ӵ��ʷ����� | |
| D�� | �κ����Ӽ����γɹ����бض��е��ӵĵ���ʧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʯ����ʹ������ɶ��� | |
| B�� | ������ˮ | |
| C�� | ������ˮ�����������˶� | |
| D�� | ̫�������������ҳ������ڣ��ɿ����Ӵ��ڵ��������һ��������ͨ· |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢۢ� | B�� | �٢ڢݢ� | C�� | �ڢۢ� | D�� | �٢ڢۢܢݢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʱ��/min | 0 | 10 | 20 | 30 | 40 |
| n��C8H10��/mol | 0.40 | 0.30 | 0.26 | n2[��Դ��] | n3 |
| n��C8H8��/mol | 0.00 | 0.10 | n1 | 0.16 | 0.16 |
| ��ѧ�� | C-H | C-C | C=C | H-H |
| ����/kJ•mol?1 | 412.5 | 348 | 612 | 436 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  �����е�K+����ZnSO4��Һ | |
| B�� | 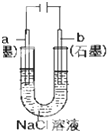 ����һ��ʱ���a��������Һ��C��OH-������ | |
| C�� | 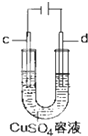 ����ʱ��c��Ϊ����������Ӧ | |
| D�� |  ������Zn����Fe��װ������Fe2+���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com