
下列事实中,与电化学腐蚀无关的是
A.在空气中,光亮的银表面逐渐变暗
B.为保护海轮的船壳,常在船壳上镶入锌块
C.埋在潮湿土壤里的铁管比埋在干燥土壤里的铁管更易被腐蚀
D.镀锡的铁制品,镀层部分受损后,露出的铁表面易被腐蚀
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2014-2015学年江西省高三上学期第六次考试理综化学试卷(解析版) 题型:填空题
近年来,为提高能源利用率,西方提出共生理念——为提高经济效益,人类生产活动尽可能多功能化。共生工程将会大大促进化学工业的发展。
(1)由于共生工程的应用,利用发电厂产生的SO2制成自发电池,其电池反应方程式为:2SO2+O2+2H2O=2H2SO4,该电池电动势为1.06V。实际过程中,将SO2通入电池的 极(填“正”或“负”),负极反应式为 ;用这种方法处理SO2废气的优点是 。
(2)以硫酸工业的SO2尾气、氨水、石灰石、焦炭、碳酸氢铵和氯化钾等为原料,可以合成有重要应用价值的硫化钙、硫酸钾、亚硫酸铵等物质。合成路线如下:
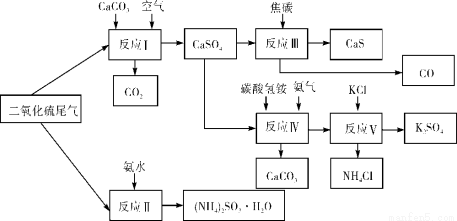
① 生产中,向反应II中的溶液中加入适量还原性很强的对苯二酚等物质,其目的是 。
② 下列有关说法正确的是 (填序号)。
A.反应Ⅰ中需鼓入足量空气,以保证二氧化硫充分氧化生成硫酸钙
B.反应III中发生反应的化学方程式为CaSO4+4C  CaS+4CO↑
CaS+4CO↑
C.反应IV需控制在60~70℃,目的之一是减少碳酸氢铵的分解
D.反应V中的副产物氯化铵可用作氮肥
③ 反应V中选用了40%的乙二醇溶液做溶剂,温度控制在25℃,此时硫酸钾的产率
超过90%,选用40%的乙二醇溶液做溶剂的原因是 。
④(NH4)2SO3可用于电厂等烟道气中脱氮,将氮氧化物转化为氮气,同时生成一种氮肥,形成共生系统。写出二氧化氮与亚硫酸铵反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高一上第二次月考化学试卷(解析版) 题型:推断题
下图中A~J均为中学化学中常见的物质.它们之间有如下转化关系。其中,A、D为金属单质,A元素是地壳中含量最多的金属元素(反应过程中生成的水及其它产物己略去)

请回答以下问题:
(1)B是______,H是________(填化学式)。
(2)写出A直接转化为F的离子反应方程式:_____________。
(3)写出E与过量氨水反应的离子反应方程式:_______________。
(4)H在空气中转化为I 的化学反应方程式:__________________。
(5)写出A与B高温下发生的化学反应方程式__________________。
(6)用一个离子方程式表示E转化为F___________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高一上期末模拟化学试卷(解析版) 题型:选择题
下列属于电解质的是
A.NaCl溶液 B.蔗糖 C.CuSO4·5H2O D.CO2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高二上第三次月考化学试卷(解析版) 题型:填空题
合成氨技术的发明使工业化人工固氮成为现实。
(1)已知N2(g)+3H2(g) 2NH3(g) ΔH=-92.2 kJ·mol-1。在一定条件下反应时,当生成标准状况下33.6 L NH3时,放出的热量为________。
2NH3(g) ΔH=-92.2 kJ·mol-1。在一定条件下反应时,当生成标准状况下33.6 L NH3时,放出的热量为________。
(2)合成氨混合体系在平衡状态时NH3的百分含量与温度的关系如图所示。由图可知:

①温度T1、T2时的平衡常数分别为K1、K2,则K1__________K2 (填“>”或“<”)。若在恒温、恒压条件下,向平衡体系中通入氦气,平衡__________移动(填“向左”、“向右”或“不”)。
②见右图,T2温度时,在1 L的密闭容器中加入2.1 mol N2、1.5 mol H2,经10 min达到平衡,则v(H2)=________mol/ (L.min)达到平衡后,如果再向该容器内通入N2、H2、NH3各0.4 mol,则平衡________移动(填“向左”、“向右”或“不”)。
(3)工业上用CO2和NH3反应生成尿素:CO2(g)+2NH3(g) H2O(l)+CO(NH2)2(l) ΔH,在一定压强下测得如下数据:
H2O(l)+CO(NH2)2(l) ΔH,在一定压强下测得如下数据:

①则该反应ΔH______0,表中数据a______d,b______f(均选填“>”、“=”或“<”)。
②从尿素合成塔内出来的气体中仍含有一定量的CO2、NH3,应如何处理?_________________。
查看答案和解析>>
科目:高中化学 来源:2016届安徽省高三上第四次月考化学试卷(解析版) 题型:填空题
元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2。元素Y基态原子的3p轨道上有4个电子。元素Z的原子最外层电子数是其内层的3倍。
(1)X与Y所形成化合物晶体的晶胞如图所示。
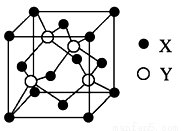
①在一个晶胞中,X离子的数目______;
②该化合物的化学式为______________;
(2)在Y的氢化物(H2Y)分子中,Y原子轨道的杂化类型是____________;
(3)Z的氢化物(H2Z)在乙醇中的溶解度大于H2Y,其原因是____________;
(4)Y与Z可形成YZ42-。
①YZ42-的空间构型为____________(用文字描述);
②写出一种与YZ42-互为等电子体的分子的化学式____________;
(5)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1mol该配合物中含有δ键的数目为________;
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省高三上期末理综化学试卷(解析版) 题型:选择题
下列实验操作与实验目的或结论一致的是
选项 | 实验操作 | 实验目的或结论 |
A | 取酸雨试样,加入10%H2O2溶液,再加入BaCl2溶液,有白色沉淀生成 | 该酸雨试样中一定含有H2SO4 |
B | 将锌片和银片用导线连接后同时插入盛有稀硫酸的烧杯中,银片表面产生大量气泡 | 形成的原电池中锌作负极,银作正极 |
C | 某无色溶液,加银氨溶液,水浴加热,有银镜生成 | 溶液中一定含有醛类化合物 |
D | 配制FeCl2溶液时,先将FeCl2溶于适量稀硝酸,再用蒸馏水稀释,最后在试剂瓶中加入少量的铁粉 | 抑制Fe 2+水解,并防止Fe 2+被氧化为Fe3+ |
查看答案和解析>>
科目:高中化学 来源:2016届陕西省高三上12月模拟化学试卷(解析版) 题型:选择题
下列有关元素化合物的说法正确的是
A.常温下,1mol铜片投入含有4mol HNO3的浓硝酸中,铜片可以完全溶解
B.Al与S直接化合可以得到Al2S3,Fe与S直接化合也可以得到Fe2S3
C.电解AlCl3、FeCl3、CuCl2的混合溶液中,阴极上依次析出Al、Fe、Cu
D.等质量的钠铝合金中铝的含量越大,与足量盐酸反应时放出的氢气越少
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高一上学期12月月考化学试卷(解析版) 题型:推断题
下列框图中的物质均为中学化学中常见物质,其中甲、乙为单质,其余均为化合物,B为常见液态化合物,A为淡黄色固体,F、G所含元素相同且均为氯化物,G遇KSCN溶液显红色。
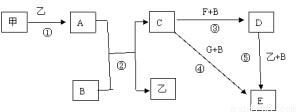
请问答下列问题:
(1)A是____________,G是______________。(填化学式)
(2)反应①-⑤中,属于氧化还原反应的是________________(填序号)。
(3)反应⑤的化学方程式为_________________________。
甲与B反应的离子方程式 ___________________________。
(4)在实验室将C溶液滴入F溶液中,观察到的现象是___________________。
(5)在F溶液中加入等物质的量的A,发生反应的总的离子方程式: ____________________。
(6)已知:酚酞在c(OH-) 为1.0×10-4mol/L~2.5mol/L时呈红色,且半分钟内不褪色。向3.9g A和 100g B混合后的溶液中滴入2滴酚酞试液,溶液变红色,片刻红色褪去。(假设过程中液体体积不变)①甲同学认为“红色迅速褪去”是由于溶液中c(OH-)过大造成的。
上述观点是否正确 ,请通过计算对比数据加以说明_____________________。
②乙同学认为“红色迅速褪去”是由于A + B = 碱 + H2O2 ,H2O2具有氧化性和漂白性导致的。试设计简单实验证明烧瓶内溶液中含H2O2,简述实验原理 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com