
| A. | 因海水中蕴藏着极其丰富的碘元素,所以工业上也可以直接用海水来提取碘元素 | |
| B. | 碱化操作时,加入NaOH溶液的原因是在碱性溶液中,可溶性有机质可形成沉淀 | |
| C. | 在实验室进行氧化操作时,加入的氧化剂可以是新制氯水、双氧水等 | |
| D. | 在实验室进行过滤操作时,需要用到玻璃仪器有玻璃棒、烧杯、漏斗 |
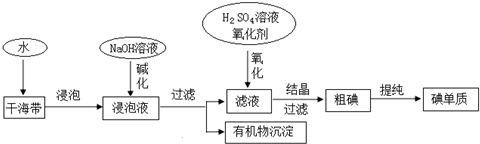
分析 从海带中提取碘:海带浸泡后加碱进行碱化,过滤得到有机沉沉物,滤液加入氧化剂和稀硫酸氧化碘离子为碘单质,得到含碘水溶液,加入有机溶剂,萃取分液得到含碘的有机溶液,通过蒸馏得到碘单质.A.海带中含有碘元素,主要以碘离子(I-)的形式存在;
B.依据从海带中提取碘的工业生产过程分析;
C.海水中含有大量的氯化钠,加入氧化剂氯水不引入杂质,双氧水被还原后的产物为水,也不引入杂质;
D.过滤是除去液体中混有的固体物质的一种方法,过滤用到的玻璃仪器有:烧杯、漏斗、玻璃棒.
解答 解:A.工业上用来提取碘元素,主要来自于海生植物海带,不可以直接用海水来提取碘元素,故A错误;
B.从海带中提取碘工业流程可知:海带浸泡后加碱进行碱化,过滤得到有机沉沉物,故B正确;
C.提取海带中碘元素时,为保证I-完全氧化为I2,加入的氧化剂H2O2,双氧水被还原后的产物为水,不引入杂质,加入的氧化剂也可以是新制氯水,氯气可将碘离子氧化为碘单质,反应的离子方程式为2I-+Cl2=2Cl-+I2,故C正确;
D.过滤时需要制作过滤器的漏斗、固定仪器的铁架台、引流用的玻璃棒、承接滤液的烧杯,故D正确;
故选A.
点评 本题考查从海带中提取碘的工业生产过程,涉及物质的分离、提纯的方法及选择、海水资源利用等,把握物质的性质及性质差异为解答的关键,注意实验的评价性分析,题目难度不大.


科目:高中化学 来源: 题型:解答题


 ;壬的结构简式
;壬的结构简式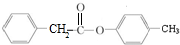


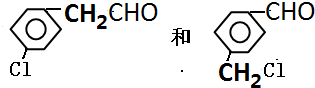 (任写一种)
(任写一种)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤的气化和液化是物理变化,煤的干馏是化学变化 | |
| B. | 乙醇、过氧化氢、次氯酸钠等消毒液均可以将病毒氧化而达到消毒的目的 | |
| C. | 氢氧燃料电池发电,比氢气直接在空气中燃烧发电能量转换率高 | |
| D. | 合成氨反应N2(g)+3H2(g)?2NH3(g) OH<O,加入催化剂能加快反应速率并提高转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分别加入Na0H溶液并加热,鉴别地沟油(餐饮废弃油)和矿物油(汽油、煤油等) | |
| B. | 为检验酸性溶液中的Cl-和SO42-,先加硝酸银溶液,滤去沉淀后加硝酸钡溶液 | |
| C. | 为探究温度对化学反应速率的影响时,先将硫代硫酸钠与硫酸两种溶液混合后再用水浴加热 | |
| D. | 往含有FeBr2和FeI2的混合溶液中通足量的氯气,然后把溶液蒸干、灼烧,得到FeCl3固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
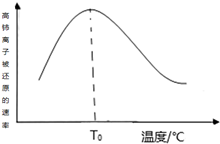 高铈离子被还原的速率与温度的关系如图所示.图象中,温度高于T0时,高铈离子被还原的速率逐渐减小的原因是高铈离子被还原的反应,正反应为放热反应,开始反应时,反应物浓度大,反应速率快,正反应为放热反应,温度逐渐升高,反应速率加快,温度高于T0℃时,反应物的浓度减少,反应速率减小,温度对反应速率的影响不及浓度的影响.
高铈离子被还原的速率与温度的关系如图所示.图象中,温度高于T0时,高铈离子被还原的速率逐渐减小的原因是高铈离子被还原的反应,正反应为放热反应,开始反应时,反应物浓度大,反应速率快,正反应为放热反应,温度逐渐升高,反应速率加快,温度高于T0℃时,反应物的浓度减少,反应速率减小,温度对反应速率的影响不及浓度的影响.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
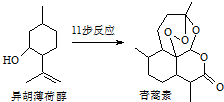 2015年诺贝尔生理学、医学奖的一半授予我国药物化学家屠吆吆,以表彰她发明抗疟疾新药青蒿素和双氢青蒿素.以异胡薄荷醇为起始原料是人工全合成青蒿素的途径之一(如图).下列说法正确的是( )
2015年诺贝尔生理学、医学奖的一半授予我国药物化学家屠吆吆,以表彰她发明抗疟疾新药青蒿素和双氢青蒿素.以异胡薄荷醇为起始原料是人工全合成青蒿素的途径之一(如图).下列说法正确的是( )| A. | 异胡薄荷醇的分子式为C10H12O | |
| B. | 青蒿素提取时可以通过加热或加碱溶解的方法提高其浸取率 | |
| C. | 青蒿素易溶于水,而难溶于有机溶剂 | |
| D. | 异胡薄荷醇可发生消去反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 汽油中绝不含铅元素 | B. | 汽油中不人为添加含铅元素的物质 | ||
| C. | 汽油中含铅元素在一定指标范围内 | D. | 以上都不正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 图①表示向含Mg2+、Al3+、NH4+的盐溶液中滴加NaOH溶液时,沉淀的量与NaOH的体积的关系图.则三种离子的物质的量之比为:n(Mg2+):n(Al3+):n( NH4+)=2:3:2 | |
| B. | 图①中使用的NaOH的浓度为2 mol/L | |
| C. | 图②表示25℃时,用0.1 mol•L-1盐酸滴定20 mL 0.1 mol•L-1 NaOH溶液,溶液的pH随加入酸体积的变化 | |
| D. | 图③中曲线表示3H2(g)+N2(g)═2NH3(g)反应过程的能量变化.若使用催化剂,B点会降低 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com