
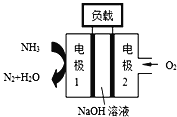
【题目】瑞典ASES公司设计的曾用于驱动潜艇的液氨﹣液氧燃料电池如图所示,该燃料电池工作时,负极的电极反应式为________;电池的总反应为________
科目:高中化学 来源: 题型:
【题目】苯巴比妥是1903年就开始使用的安眠药,其合成路线如图(部分试剂和产物略)。
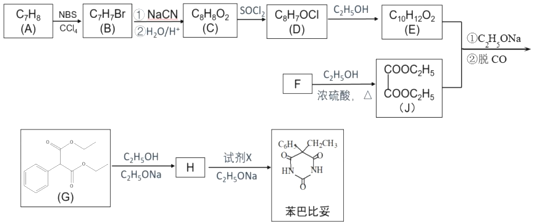
已知:①NBS是一种溴代试剂
②![]() +
+![]()
![]()
![]() + C2H5OH
+ C2H5OH
③R1—COOC2H5+![]()
![]()
![]() +C2H5OH
+C2H5OH
请回答下列问题:
(1)下列说法正确的是__________
A. 1 mol E在NaOH溶液中完全水解,需要消耗2 mol NaOH
B. 化合物C可以和FeCl3溶液发生显色反应
C. 苯巴比妥具有弱碱性
D. 试剂X可以是CO(NH2)2
(2)B中官能团的名称__________,化合物H的结构简式为_______。
(3)D→E的化学方程式为_________。
(4)苯巴比妥的一种同系物K,分子式为C10H8N2O3,写出K同时符合下列条件的同分异构体的结构简式______
①分子中含有两个六元环;且两个六元环结构和性质类似
②能够和FeCl3发生显色反应
③核磁共振氢谱显示分子中由5种氢
(5)参照流程图中的反应,设计以甲苯为原料合成聚酯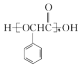 __________(用流程图表示,无机试剂任选)
__________(用流程图表示,无机试剂任选)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠(NaNO2)是一种肉制品生产中常见的食品添加剂,使用时必须严格控制其用量。在漂白、电镀等方面应用也很广泛。某兴趣小组设计了如下图所示的装置制备NaNO2(A中加热装置已略去)。
已知:室温下,①2NO+Na2O2===2NaNO2
②酸性条件下,NO 或NO2-都能与MnO4-反应生成NO3-和Mn2+
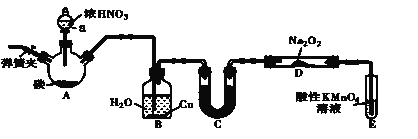
(1)A中发生反应的化学方程式为_________________________________。
(2)检查完该装置的气密性,装入药品后,实验开始前通入一段时间N2,然后关闭弹簧夹,再滴加浓硝酸,加热。通入N 2的作用是______________。
(3)装置B中观察到的主要现象为_________________
(4)①为保证制得的亚硝酸钠的纯度,C装置中盛放的试剂可能是___________(填字母序号)。
A.P2O5 B.无水CaCl2 C.碱石灰 D.浓硫酸
②如果取消C装置,D中固体产物除NaNO2外,可能含有的副产物有________ 写化学式)。
(5)E中发生反应的离子方程式为____________。
(6)将1.56g Na2O2完全转化为NaNO2,理论上至少需要木炭__________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.标准状况下,11.2LH2与11.2LD2所含的质子数均为NA
B.硅晶体中,有NA个Si原子就有4NA个Si—Si键
C.6.4g Cu与3.2g硫粉混合隔绝空气加热,充分反应后,转移电子书为0.2NA
D.用惰性电极电解食盐水,若导线中通过2NA个电子,则阳极产生22.4L气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在固态金属氧化物电解池中,高温共电解H2O—CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示。下列说法不正确的是( )
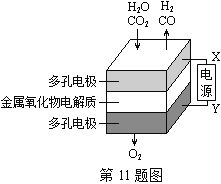
A. X是电源的负极
B. 阴极的反应式是:H2O+2eˉ=H2+O2ˉCO2+2eˉ=CO+O2ˉ
C. 总反应可表示为:H2O+CO2H2+CO+O2
D. 阴、阳两极生成的气体的物质的量之比是1︰1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】数依次增大的四种元素A、B、C、D分别处于第一至第四周期,自然界中存在多种A的化合物,B原子核外电子有6种不同的运动状态,B与C可形成正四面体形分子,D的基态原子的最外能层只有一个电子,其他能层均已充满电子。请回答下列问题:
(1)这四种元素中电负性最大的元素,其基态原子的价电子排布图为___________________,第一电离能最小的元素是__________(填元素符号)。
(2)C所在主族的前四种元素分别与A形成的化合物,沸点由高到低的顺序是___________(填化学式)。
(3)B元素可形成多种单质,一种晶体结构如图一所示,其原子的杂化类型为__________;另一种的晶胞如图二所示,该晶胞的空间利用率为__________。(![]() =1.732)
=1.732)
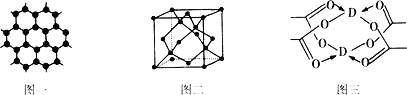
(4)D元素形成的单质,其晶体的堆积模型为__________,D的醋酸盐晶体局部结构如图三,该晶体中含有的化学键是__________ (填选项序号)。
①极性键 ②非极性键 ③配位键 ④金属键
(5)向D的硫酸盐溶液中滴加过量氨水,观察到的现象是______________________________。
请写出上述过程的离子方程式:___________________________,__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 是一种常见的化学试剂,是制备其他含锰化合物的重要原料。某课外化学兴趣小组利用软锰矿
是一种常见的化学试剂,是制备其他含锰化合物的重要原料。某课外化学兴趣小组利用软锰矿![]() 主要成分为
主要成分为![]() ,含少量
,含少量![]() 、
、![]() 和
和![]() 制备
制备![]() ,设计流程如图:
,设计流程如图:![]() 注:试剂①②③按编号顺序加入
注:试剂①②③按编号顺序加入![]()

已知:常温时部分难溶化合物的![]() 近似值
近似值![]() 如表:
如表:
物质 |
|
|
|
|
|
|
|
|
|
|
|
(1)该小组同学在酸浸之前,先将软锰矿粉碎,其目的是________。
(2)“酸浸”过程中![]() 发生反应的离子方程式为________。
发生反应的离子方程式为________。
(3)加入![]() 固体的作用是________,甲同学提出将上述流程中的氨水换成氢氧化钠溶液,乙同学觉得不妥,乙同学的理由是________。
固体的作用是________,甲同学提出将上述流程中的氨水换成氢氧化钠溶液,乙同学觉得不妥,乙同学的理由是________。
(4)丙同学认为向滤液C中滴加![]() 溶液的过程中可能会生成
溶液的过程中可能会生成![]() 沉淀,并提出可能的原因为
沉淀,并提出可能的原因为![]() ,常温时,该反应的平衡常数
,常温时,该反应的平衡常数![]() ________
________![]() 填数值
填数值![]() 。
。![]() 已知
已知![]() ,
,![]() 。
。
(5)操作Ⅰ的名称为________。
(6)如图是小组同学将![]() 晶体放在坩埚里加热分解时,固体失重质量分数随温度
晶体放在坩埚里加热分解时,固体失重质量分数随温度![]() 变化的曲线
变化的曲线![]() 已知草酸锰不稳定,但其中锰元素的化合价在
已知草酸锰不稳定,但其中锰元素的化合价在![]() 以下不变
以下不变![]() 。
。
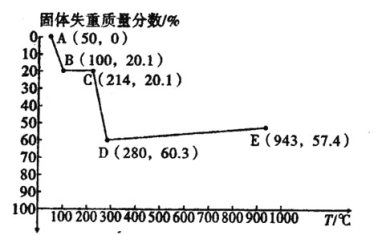
试根据各点的坐标![]() 近似值
近似值![]() 回答下列问题:
回答下列问题:
①![]() 的化学方程式为________。
的化学方程式为________。
②从D点到E点过程中固体失重的质量分数下降的原因是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】油脂是重要的营养物质.某天然油脂A可发生下列反应:
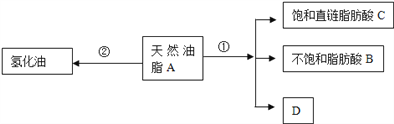
已知:A的分子式为C57H106O6.1mol该天然油脂A经反应①可得到1molD、1mol不饱和脂肪酸B和2mol直链饱和脂肪酸C.经测定B的相对分子质量为280,原子个数比为C:H:O=9:16:1;
(1)写出B的分子式:________________________;
(2)写出反应①的反应类型:____________;C的名称(或俗称)是_________;
(3)近日,电视媒体关于“氢化油危害堪比杀虫剂”的报道引发轩然大波,反应②为天然油脂的氢化过程.下列有关说法不正确的是_______________;
a.氢化油又称人造奶油,通常又叫硬化油.
b.植物油经过氢化处理后会产生副产品反式脂肪酸甘油酯,摄入过多的氢化油,容易堵塞血管而导致心脑血管疾病.
c.氢化油的制备原理是在加热植物油时,加入金属催化剂,通入氢气,使液态油脂变为半固态或固态油脂.
d.油脂的氢化与油脂的皂化都属于加成反应
(4)D和足量金属钠反应的化学方程式_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如图所示变化规律(p表示压强,T表示温度,n表示物质的量):根据以上规律判断,下列结论正确的是( )
A. 反应Ⅰ:△H>0,p2>p1
反应Ⅰ:△H>0,p2>p1
B. 反应Ⅱ:△H>0,T1>T2
反应Ⅱ:△H>0,T1>T2
C. 反应Ⅲ:△H>0,T2>T1或△H<0,T2<T1
反应Ⅲ:△H>0,T2>T1或△H<0,T2<T1
D. 反应Ⅳ:△H<0,T2>T1
反应Ⅳ:△H<0,T2>T1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com