
 �ǻ���ʯ[Ca5��PO4��3OH]��һ����Ҫ�����������ϣ��䳣�õ��Ʊ����������֣�
�ǻ���ʯ[Ca5��PO4��3OH]��һ����Ҫ�����������ϣ��䳣�õ��Ʊ����������֣����� ��1���ٴ������غ�ĽǶ�˼����5molCa��NO3��2��3mol��NH4��2HPO4��4molNH3•H2O��Ӧ����1molCa5��PO4��3OH��10molNH4NO3��3molH2O���ݴ���д����ʽ��
�������غ�ĽǶ�˼����5molCa��OH��2��3molH3PO4��Ӧ����1molCa5��PO4��3OH��9molH2O��
��2������A�뷽��B�Աȣ���Ҫ��A�����и�����NH4NO3��ԭ�������ʲ��ߣ�
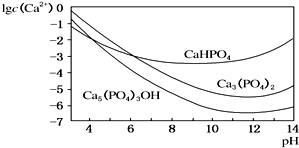
��3������ͼ֪����֪����Һ����Խǿ��Խ��������CaHPO4��
��4������pH��������7.39��7.41�����Ը���Ҫ������ʽΪCa5��PO4��3OH��
��5����Ӧƽ�⣺Ca5��PO4��3OH��s��?5Ca2+��aq��+3PO43-��aq��+OH-��aq������������ʹ�����ܽ������ƶ���
��� �⣺��1���ٴ������غ�ĽǶ�˼����5molCa��NO3��2��3mol��NH4��2HPO4��4molNH3•H2O��Ӧ����1molCa5��PO4��3OH��10molNH4NO3��3molH2O����Ӧ�Ļ�ѧ����ʽΪ��5Ca��NO3��2+3��NH4��2HPO4+4NH3•H2O=Ca5��PO4��3OH��+10NH4NO3+3H2O
�ʴ�Ϊ��10NH4NO3��3H2O��
�ڴ������غ�ĽǶ�˼����5molCa��OH��2��3molH3PO4��Ӧ����1molCa5��PO4��3OH��9molH2O��
��Ӧ�Ļ�ѧ����ʽΪ5Ca��OH��2+3H3PO4=Ca5��PO4��3OH��+9H2O��
�ʴ�Ϊ��Ca5��PO4��3OH��+9H2O��
��2���뷽��A��ȣ�����B���ŵ��Ǹ���ƷΪˮ��û����������Ʒ�����ռ�
�ʴ�Ϊ��Ψһ������Ϊˮ�����ռ�
��3������B�У����H3PO4��Һ�μӹ��죬�ᵼ�¾ֲ����Թ�������CaHPO4���ƵõIJ��ﲻ����
�ʴ�Ϊ����ӦҺ�ֲ����Թ�����CaHPO4������
��4������pH��������7.39��7.41�����Ը���Ҫ������ʽΪCa5��PO4��3OH��
�ʴ�Ϊ��Ca5��PO4��3OH��
��5����Ӧƽ�⣺Ca5��PO4��3OH��s��?5Ca2+��aq��+3PO43-��aq��+OH-��aq������������ʹ�����ܽ������ƶ�������Ca5��PO4��3OH�ܽ⣬���ȣ�ݣ�
�ʴ�Ϊ����������ʹ�����ܽ�ƽ�⣬Ca5��PO4��3OH��s��?5Ca2+��aq��+3PO43-��aq��+OH-��aq�������ƶ�������Ca5��PO4��3OH�ܽ⣬���ȣ�ݣ�
���� ���⿼���Ʊ�ʵ�鷽����Ƽ���������ܽ�ƽ�⣬Ϊ��Ƶ���㣬��ȷ�������ʼ�ͼ�����ߺ����ǽⱾ��ؼ������ؿ���ѧ����ȡ��Ϣ������Ϣ��������������ѵ���ͼ�����ݵ�������ã���Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ������ˮ�����ˮ����ɫ��dz | |
| B�� | �ѻ���������ˮ�����ˮ����ɫ��dz | |
| C�� | ��ϩ��ˮ��һ�������·�Ӧ��ȡ�Ҵ� | |
| D�� | ������������һ�������·�Ӧ��ȡ��һ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��ʼ������pH | ������ȫ��pH | |
| Fe3+ | 1.1 | 3.2 |
| Mn2+ | 8.3 | 9.8 |
| Cu2+ | 4.4 | 6.4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2 4 3 2 2 6 | B�� | 0 2 1 0 1 2 | ||
| C�� | 2 0 1 2 0 2 | D�� | 2 2 2 2 1 4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���� | |
| B�� | ����100 mL 0.1 mol•L-1�Ĵ�����Һ | |
| C�� | ����������0.5 mol•L-1������ | |
| D�� | ����������1 mol•L-1��NaOH��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��NaOH��Һ������NH4Cl��KCl | |
| B�� | �������ữ��AgNO3��Һ������NH4Cl��NH4NO3 | |
| C�� | ij��Һ�еμ�BaCl2��Һ�������ɫ�����������Һ��һ������SO42-���� | |
| D�� | ����ɫ��Ӧ����NaCl��KNO3 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com