
下列依据热化学方程式得出的结论正确的是( )
A.若2H2(g)+O2(g) ===2H2O(g) ΔH=-483.6 kJ·mol-1,则1 mol H2 燃烧放出热量
为241.8 kJ·mol-1
B.若C(石墨,s) ===C(金刚石,s) ΔH > 0,则石墨比金刚石稳定
C.已知NaOH(aq)+HCl(aq )===NaCl(aq)+H2O(l) ΔH=-57.4 kJ·mol-1,
)===NaCl(aq)+H2O(l) ΔH=-57.4 kJ·mol-1,
则20.0g NaOH 固体与稀盐酸完全中和,放出28.7 kJ的热量
固体与稀盐酸完全中和,放出28.7 kJ的热量
D. 已知2C(s)+2O2(g) ===2CO2(g) ΔH1;2C(s)+O2(g) =2CO(g) ΔH2,则ΔH1>ΔH2
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案科目:高中化学 来源: 题型:
在第n层电子层中,当n为最外层时容纳的电子数最多与n-1层相同;当它为原子的次外层时,其电子数比n+1层最多能多10个电子,则n层为( )
A.N层 B.M层
C.L层 D.K层
查看答案和解析>>
科目:高中化学 来源: 题型:
某醇的分子式为CnH2n+1OH,该醇2.3 g与足量的金属钠反应,生成氢气0.56 L(标准状况),则此醇的相对分子质量是( )
A.92 B.69
C.46 D.32
查看答案和解析>>
科目:高中化学 来源: 题型:
根据元素周期表判断,下列叙述不正确的是( )
A.K层电子为奇数的所有元素所在族的序数与该元素原子的K层电子数相等
B.L层电子为奇数的所有元素所在族的序数与该元素原子的L层电子数相等
C.L层电子为偶数的所有主族元素所在族的序数与该元素原子的L层电子数相等
D.M层电子为奇数的所有主族元素所在族的序数与该元素原子的M层电子数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关化学能量的说法不正确的是( )
A. 中和反应都是放热反应
B.能自发进行的反应都是放热反应
C.化学反应除了生成新物质外,一定伴随着能量变化
D. 吸热反应中反应物的总能量一定小于生成物的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
下列操作会导致实验结果偏高的是( )
A.中和热测定实验中,用铜制搅拌器进行搅拌,所测中和热的数值
B.配制一定物质的量浓度的溶液时,用量筒量取浓溶液的体积时仰视读数,所配溶液的浓度
C.中和滴定测定盐酸溶液浓度,量取20.00mL待测盐酸溶液的滴定管未用待测盐酸溶液润洗
D.用托盘天平称量10.5g某物质,砝码和药品的位置放反,所称药品的质量
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C三种强电解质,它们在水中电离出的离子
如右表所示:
| 阳离子 | Ag+、Na+ |
| 阴离子 | NO3-、SO42-、Cl- |
下图Ⅰ所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A、 B、 C三种溶液,电极均为石墨电极。接通电源,经过一段时间后,测得乙中c电极质量增加了27 g。常温下各烧杯中溶液的pH与电解时间t的关系如下图Ⅱ所示。据此回答下列问题:
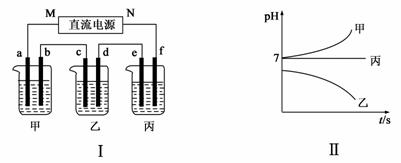
(1)M为电源的________(填“正”或“负”)极,A是________(填写化学式)。
(2)计算电极f上生成的气体在标准状况下的体积: 。
(3)写出b电极上发生的电极反应 ;
写出乙烧杯的电解池反应:_________________________________ 。
(4)要使丙恢复到原来的状态,应加入 g (填写化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学欲探究SO2的还原性和酸性氧化物的性质,设计了如下实验:
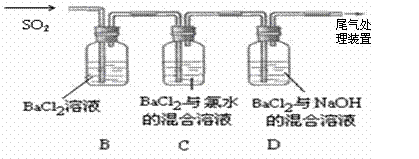 |
先通入N2,将装置中的空气排净,然后通入SO2。请回答:
(1)B中的现象是 。
(2)C中的现象是 ,
出现该现象的原因是
(用离子方程式表示)。
(3)D中的现象是 ,
出现该现象的原因是
(用离子方程式表示)。
(4)通过上述实验得出的结论是:SO2与BaCl2溶液在 或 条件下会生成沉淀。
查看答案和解析>>
科目:高中化学 来源: 题型:
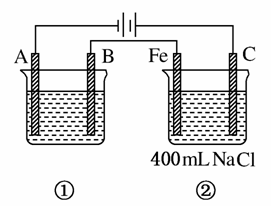
如图为相互串联的①、②两电解池。试回答:
(1)若①池利用电解原理在铁上镀银,则A是________、________(填电极材料和电极名称),电极反应式是__________________;B(要求同A)是________、________,电极反应式是___________________,选用的电解质溶液是________溶液。
(2)②池中若滴入少量酚酞试液,电解一段时间后,铁极附近呈______色,C极附近呈______色。
(3)若①池阴极增重43.2 g,则②池中阳极上放出的气体在标准状况下的体积是________mL。若②池中剩余溶液仍为400 mL,则电解后所得溶液的物质的量浓度为________mol·L-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com