
ФЪ298 KЎў1.01ЎБ105 PaПВ,Ѕ«22 g CO2НЁИл750 mL 1 molЎ¤L-1NaOHИЬТєЦРід·Ц·ґУ¦,ІвµГ·ґУ¦·Еіцx kJµДИИБїЎЈТСЦЄФЪёГМхјюПВ,1 mol CO2НЁИл1 L 2 molЎ¤L-1 NaOHИЬТєЦРід·Ц·ґУ¦·Еіцy kJµДИИБїЎЈФтCO2УлNaOHИЬТє·ґУ¦ЙъіЙNaHCO3µДИИ»ЇС§·ЅіМКЅОЄ(ЎЎЎЎ)
A.CO2(g)+NaOH(aq) NaHCO3(aq) ¦¤H=-(2y-x)kJЎ¤mol-1
NaHCO3(aq) ¦¤H=-(2y-x)kJЎ¤mol-1
B.CO2(g)+NaOH(aq) NaHCO3(aq) ¦¤H=-(2x-y)kJЎ¤mol-1
NaHCO3(aq) ¦¤H=-(2x-y)kJЎ¤mol-1
C.CO2(g)+NaOH(aq) NaHCO3(aq) ¦¤H=-(4x-y)kJЎ¤mol-1
NaHCO3(aq) ¦¤H=-(4x-y)kJЎ¤mol-1
D.CO2(g)+NaOH(aq) NaHCO3(aq) ¦¤H=-(8x-2y)kJЎ¤mol-1
NaHCO3(aq) ¦¤H=-(8x-2y)kJЎ¤mol-1
C
ЎѕЅвОцЎїёщѕЭ·ґУ¦CO2+NaOH NaHCO3ЎўCO2+2NaOH
NaHCO3ЎўCO2+2NaOH Na2CO3+H2O,Фт22 g CO2НЁИл750 mL 1 molЎ¤L-1 NaOHИЬТєЦРід·Ц·ґУ¦ІъОпОЄNaHCO3ЎўNa2CO3µД»мєПОпЎЈЙиІОјУ·ґУ¦ЙъіЙNaHCO3µДCO2ОпЦКµДБїОЄa,ІОјУ·ґУ¦ЙъіЙNa2CO3µДCO2ОпЦКµДБїОЄb,Фтa+b=0.5 mol,a+2b=0.75 mol,ЅвµГ:a=b=0.25 molЎЈёщѕЭИИБїБР№ШПµ,ЙПКц·ґУ¦ЦРІъЙъ0.25 mol NaHCO3·ЕіцµДИИБїОЄ(x-0.25y)kJ,№КСЎCПоЎЈ
Na2CO3+H2O,Фт22 g CO2НЁИл750 mL 1 molЎ¤L-1 NaOHИЬТєЦРід·Ц·ґУ¦ІъОпОЄNaHCO3ЎўNa2CO3µД»мєПОпЎЈЙиІОјУ·ґУ¦ЙъіЙNaHCO3µДCO2ОпЦКµДБїОЄa,ІОјУ·ґУ¦ЙъіЙNa2CO3µДCO2ОпЦКµДБїОЄb,Фтa+b=0.5 mol,a+2b=0.75 mol,ЅвµГ:a=b=0.25 molЎЈёщѕЭИИБїБР№ШПµ,ЙПКц·ґУ¦ЦРІъЙъ0.25 mol NaHCO3·ЕіцµДИИБїОЄ(x-0.25y)kJ,№КСЎCПоЎЈ


 °ЩДкС§µдїОК±С§Б·ІвПµБРґр°ё
°ЩДкС§µдїОК±С§Б·ІвПµБРґр°ё ИК°®УўУпН¬ІЅБ·П°ІбПµБРґр°ё
ИК°®УўУпН¬ІЅБ·П°ІбПµБРґр°ё
| Дкј¶ | ёЯЦРїОіМ | Дкј¶ | іхЦРїОіМ |
| ёЯТ» | ёЯТ»Гв·СїОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СїОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СїОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СїОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СїОіМНЖјцЈЎ | іхИэ | іхИэГв·СїОіМНЖјцЈЎ |
їЖДїЈєёЯЦР»ЇС§ АґФґЈє2014ёЯїј»ЇС§ГыК¦ЦЄК¶µгѕ«±а СЎРЮ3ОпЦКЅб№№УлРФЦКБ·П°ѕнЈЁЅвОц°жЈ© МвРНЈєСЎФсМв
ГА№ъLawreceLiremore№ъјТКµСйКТ(LLNL)µДV.Lota.C.S.YooєНCynnіЙ№¦µШФЪёЯС№ПВЅ«CO2ЧЄ»ЇОЄѕЯУРАаЛЖSiO2Ѕб№№µДФЧУѕ§Ме,ПВБР№ШУЪCO2µДФЧУѕ§МеЛµ·ЁЦРХэИ·µДКЗ(ЎЎЎЎ)
A.CO2µДФЧУѕ§МеЦРґжФЪ·¶µВ»ЄБ¦,Гї1 mol CO2ФЧУѕ§МеЦРє¬УР2NA¦Рјь
B.ФЪТ»¶ЁМхјюПВ,CO2ФЧУѕ§МеЧЄ»ЇОЄCO2·ЦЧУѕ§МеКЗОпАн±д»Ї
C.ИЫµг:ЅрёХКЇ>ФЧУѕ§МеCO2
D.ФЪCO2µДФЧУѕ§МеЦР,ГїёцCФЧУЦЬО§ЅбєП4ёцOФЧУ,ГїёцOФЧУУлБЅёцCФЧУПаЅбєП
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє2014ёЯїј»ЇС§ГыК¦ЦЄК¶µгѕ«±а ЧЁМв8»ЇС§·ґУ¦ЛЩВКУл»ЇС§ЖЅєвБ·П°ѕнЈЁЅвОц°жЈ© МвРНЈєМоїХМв
Т»¶ЁОВ¶ИПВ,ФЪ2 LµДГЬ±ХИЭЖчЦР,XЎўYЎўZИэЦЦЖшМеµДБїЛжК±јд±д»ЇµДЗъПЯИзНјЛщКѕ:
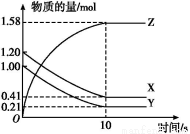
(1)ґУ·ґУ¦їЄКјµЅ10 sК±,УГZ±нКѕµД·ґУ¦ЛЩВКОЄЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ,XµДОпЦКµДБїЕЁ¶ИјхЙЩБЛЎЎЎЎЎЎЎЎ,YµДЧЄ»ЇВКОЄЎЎЎЎЎЈ
(2)ёГ·ґУ¦µД»ЇС§·ЅіМКЅОЄЎЎ
(3)10 sєуµДДіТ»К±їМ(t1)ёД±дБЛНвЅзМхјю,ЖдЛЩВКЛжК±јдµД±д»ЇНјПсИзНјЛщКѕ:
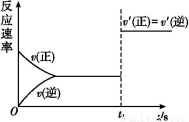
ФтПВБРЛµ·Ё·ыєПёГНјПсµДКЗЎЎЎЎЎЎЎЎЎЈ
A.t1К±їМ,ФцґуБЛXµДЕЁ¶И B.t1К±їМ,ЙэёЯБЛМеПµОВ¶И
C.t1К±їМ,ЛхРЎБЛИЭЖчМе»э D.t1К±їМ,К№УГБЛґЯ»ЇјБ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє2014ёЯїј»ЇС§ГыК¦ЦЄК¶µгѕ«±а ЧЁМв6ФЧУЅб№№»ЇС§јьБ·П°ѕнЈЁЅвОц°жЈ© МвРНЈєМоїХМв
ЛДЦЦ¶МЦЬЖЪ·ЗЅрКфФЄЛШAЎўBЎўCЎўDФЧУРтКэТАґОФцґуЎЈAКЗФЧУ°лѕ¶ЧоРЎµДФЄЛШ,BФЧУµДЧоНвІгµзЧУКэКЗґОНвІгµзЧУКэµДБЅ±¶,DФЪµШїЗЦРє¬БїЧоґуЎЈЗл»Шґр:
(1)BФЄЛШµДФЧУЅб№№КѕТвНјКЗЎЎ
(2)»ЇєПОпCA3µДµзЧУКЅКЗЎЎЎЎЎЎЎЎЎЎЎЎЎЎ,BD2·ЦЧУµДЅб№№КЅОЄЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
(3)±ыОЄє¬УРЙПКцЛДЦЦФЄЛШµДіЈјыОЮ»ъЛбКЅСО,Фт±ыµД»ЇС§КЅОЄЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЈ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє2014ёЯїј»ЇС§ГыК¦ЦЄК¶µгѕ«±а ЧЁМв6ФЧУЅб№№»ЇС§јьБ·П°ѕнЈЁЅвОц°жЈ© МвРНЈєСЎФсМв
ПВБРЛµ·ЁЦРХэИ·µДКЗ(ЎЎЎЎ)
A.ИОєОФЄЛШФЧУµДФЧУєЛ¶јКЗУЙЦКЧУєНЦРЧУ№№іЙµД
BЈ® Ўў
Ўў »ҐОЄН¬О»ЛШЈ¬
»ҐОЄН¬О»ЛШЈ¬ 2Ул
2Ул  2»ҐОЄН¬ЛШТмРОМе
2»ҐОЄН¬ЛШТмРОМе
C.іЈОВПВ,4.48 L  2є¬УР8NAёцЦРЧУ(NAОЄ°ў·ьјУµВВЮіЈКэµДЦµ)
2є¬УР8NAёцЦРЧУ(NAОЄ°ў·ьјУµВВЮіЈКэµДЦµ)
D.O2-ЎўMg2+ЎўNeµДЅб№№КѕТвНј¶јїЙТФУГ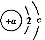 ±нКѕ
±нКѕ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє2014ёЯїј»ЇС§ГыК¦ЦЄК¶µгѕ«±а ЧЁМв5»ЇС§ДЬУлИИДЬБ·П°ѕнЈЁЅвОц°жЈ© МвРНЈєСЎФсМв
ТСЦЄјЧНйИјЙХЙъіЙ¶юСх»ЇМјєНТєМ¬Л®·ЕіцµДИИБїОЄ55.625 kJЎ¤g-1ЎЈПВБРИИ»ЇС§·ЅіМКЅЦРІ»ХэИ·µДКЗ(ЎЎЎЎ)
A.CH4(g)+2O2(g) CO2(g)+2H2O(l) ¦¤H =-890 kJ/mol
CO2(g)+2H2O(l) ¦¤H =-890 kJ/mol
B.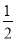 CH4(g)+O2(g)
CH4(g)+O2(g)
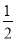 CO2(g)+H2O(l) ¦¤H=-445 kJ/mol
CO2(g)+H2O(l) ¦¤H=-445 kJ/mol
C.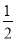 CO2(g)+H2O(l)
CO2(g)+H2O(l)
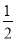 CH4(g)+O2(g) ¦¤H=+445 kJ/mol
CH4(g)+O2(g) ¦¤H=+445 kJ/mol
D.CH4(g)+2O2(g) CO2(g)+2H2O(l) ¦¤H=-55.625 kJ/mol
CO2(g)+2H2O(l) ¦¤H=-55.625 kJ/mol
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє2014ёЯїј»ЇС§ГыК¦ЦЄК¶µгѕ«±а ЧЁМв4Сх»Ї»№Ф·ґУ¦Б·П°ѕнЈЁЅвОц°жЈ© МвРНЈєМоїХМв
CuУлТ»¶ЁЕЁ¶ИµДHNO3·ґУ¦ОЄ:3Cu+2NO3ЎЄ+xH+ 3Cu2++2R+yH2OЎЈ
3Cu2++2R+yH2OЎЈ
(1)·ґУ¦ЦРµДx=ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЈ
(2)·ґУ¦ІъОпRµД»ЇС§КЅОЄЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЈ
(3)ІОјУ·ґУ¦µДCuєНПыєДHNO3µДОпЦКµДБїЦ®±ИОЄЎЎЎЎЎЎЎЎЎЎЎЈ
(4)1.5 mol CuНкИ«·ґУ¦К±ЧЄТЖµДµзЧУКэОЄЎЎЎЎЎЎЎЎЎЎЎЎЎЈ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє2014ёЯїј»ЇС§ГыК¦ЦЄК¶µгѕ«±а ЧЁМв3АлЧУ·ґУ¦Б·П°ѕнЈЁЅвОц°жЈ© МвРНЈєСЎФсМв
ПВБРёчЧйАлЧУФЪЦё¶ЁµДИЬТєЦРТ»¶ЁДЬґуБї№ІґжµДКЗ(ЎЎЎЎ)
A.ОЮЙ«ИЬТє:K+ЎўAl3+ЎўNO3ЎЄЎўAlO2ЎЄ
B.pH=12µДИЬТє:K+ЎўCl-ЎўSO32ЎЄЎўSiO32ЎЄ
C.є¬0.1 molЎ¤L-1 NO3ЎЄµДИЬТє:H+ЎўFe2+ЎўCl-ЎўSO42ЎЄ
D.УЙЛ®µзАлІъЙъµДc(H+)=1ЎБ10-12 molЎ¤L-1µДИЬТє:Na+ЎўNH4+ЎўSO42ЎЄЎўHCO3ЎЄ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє2014ёЯїј»ЇС§ГыК¦ЦЄК¶µгѕ«±а ЧЁМв21»ЇС§КµСй»щґЎБ·П°ѕнЈЁЅвОц°жЈ© МвРНЈєСЎФсМв
ПВБРЧ°ЦГєНІЩЧчДЬґпµЅКµСйДїµДµДКЗ(ЎЎЎЎ)

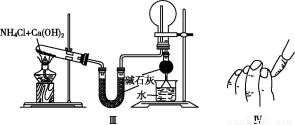
A.КµСйўс:ЦЖИЎІўКХјЇЗвЖш
B.КµСйўт:СйЦ¤ЖПМСМЗµД»№ФРФ
C.КµСйўу:КµСйКТЦЖ°±ЖшІўКХјЇёЙФпµД°±Жш
D.КµСйўф:јмІйјоКЅµО¶Ё№ЬКЗ·сВ©Тє
Ійїґґр°ёєНЅвОц>>
°Щ¶ИЦВРЕ - Б·П°ІбБР±н - КФМвБР±н
єю±±КЎ»ҐБЄНшОҐ·ЁєНІ»БјРЕПўѕЩ±ЁЖЅМЁ | НшЙПУРє¦РЕПўѕЩ±ЁЧЁЗш | µзРЕХ©ЖѕЩ±ЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРє¦РЕПўѕЩ±ЁЧЁЗш | ЙжЖуЗЦИЁѕЩ±ЁЧЁЗш
ОҐ·ЁєНІ»БјРЕПўѕЩ±Ёµз»°Јє027-86699610 ѕЩ±ЁУКПдЈє58377363@163.com