
【题目】用质量分数为98%的浓硫酸(ρ=1.84 g·cm-3)配制240 mL 1.84 mol·L-1稀硫酸,下列操作正确的是
A.将蒸馏水缓慢注入盛有一定量浓硫酸的烧杯中,并不断搅拌至冷却
B.必需的定量仪器有50 mL量筒、250 mL容量瓶和托盘天平
C.量取浓硫酸的体积为25.0 mL
D.先在容量瓶中加入适量水,将量好的浓硫酸注入容量瓶,加水定容
【答案】C
【解析】
A.浓硫酸稀释放热,故为了防止浓硫酸外溅,浓硫酸稀释时应将浓硫酸沿着烧杯壁缓缓注入水中,同时不断用玻璃棒搅拌,产生的热量及时散发出去,故A错误;
B.浓硫酸为液态,用质量分数为98%的浓硫酸(ρ=1.84 g·cm-3)配制240 mL 1.84 mol·L-1稀硫酸时,不需要用到托盘天平,故B错误;
C.质量分数为98%的浓硫酸(ρ=1.84gcm-3)物质的量浓度为![]() mol/L =18.4mol/L,设需要浓硫酸体积为V,由稀释定律可得V×18.4mol/L=250mL×1.84mol/L,解得V=25.0mL,故C正确;
mol/L =18.4mol/L,设需要浓硫酸体积为V,由稀释定律可得V×18.4mol/L=250mL×1.84mol/L,解得V=25.0mL,故C正确;
D.浓硫酸稀释放热,而容量瓶为精密仪器,不能受热,因此不能用来稀释浓硫酸,故D错误;
故选C。


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
【题目】已知短周期主族元素的离子 aA2+、bB+、cC3-、dD-都具有相同的电子层结构,下列叙述正确的是
A.离子的还原性:C3-<D-B.离子半径:C>D>B>A
C.原子序数: d>c>b>aD.单质的还原性: A>B>D>C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)将Al、Al2O3和Al(OH)3的混合物恰好与NaOH溶液反应,反应后溶液中溶质的化学式为_________。向反应后的溶液中通入少量CO2,反应的离子方程式为_______________。
(2)在100mLFeBr2溶液中通入标准状况下2.24LCl2,溶液中有1/4的Br- 被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为______________(结果保留两位小数)。
(3)三氟化氮(NF3)是一种无色无味的气体,它是微电子工业技术的关键原料之一,三氟化氮在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3,请根据要求回答下列问题:
①写出该反应的化学方程式___________________,反应中生成0.2mol HNO3,转移的电子数目为__________。
②NF3无色、无臭,但一旦在空气中泄漏,还是易于发现,判断该气体泄漏时的现象是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将![]() 缓慢通入100mL水中至饱和,然后向所得饱和氯水中逐滴加人
缓慢通入100mL水中至饱和,然后向所得饱和氯水中逐滴加人![]() 溶液,整个过程中pH的变化如图所示,下列有关叙述正确的是( )
溶液,整个过程中pH的变化如图所示,下列有关叙述正确的是( )

A.曲线③④段有离子反应:![]()
B.可依据②处数据计算所溶解的![]()
C.③处表示氯气与氢氧化钠溶液恰好反应完全
D.①处![]() 约为
约为![]() 处
处![]() 的两倍
的两倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值。下列说法正确的是
A.0.1 L 3.0 mol·L-1的NH4NO3溶液中含有的![]() 的数目为0.3NA
的数目为0.3NA
B.1.0 L 0.1 mol·L-1的NaHSO4溶液中,阳离子的数目之和为0.2NA
C.25 ℃时,pH=13的1.0 L Ba(OH)2溶液中含有的OH-数目为0.1NA
D.1 L 0.1 mol·L-1的Na2CO3溶液中所含氧原子数目为0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】稀氨水中存在着下列平衡:NH3·H2O![]() NH4++OH-,若要使平衡向逆反应方向移动,同时使c(OH-)增大,应加入的物质或采取的措施是( )
NH4++OH-,若要使平衡向逆反应方向移动,同时使c(OH-)增大,应加入的物质或采取的措施是( )
①NH4Cl固体 ②硫酸 ③NaOH固体 ④水 ⑤加热 ⑥少量MgSO4固体
A. ①②③⑤B. ③C. ③④⑥D. ③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列混合溶液中,各离子浓度的大小顺序正确的是
A. 10 mL 0.1 mol/L氨水与10 mL 0.1 mol/L盐酸混合:c(Cl)>c(![]() )>c(OH)>c(H+)
)>c(OH)>c(H+)
B. 10 mL 0.1 mol/L NH4Cl溶液与5 mL 0.2 mol/L NaOH溶液混合:c(Na+)=c(Cl)>c(OH)>c(H+)
C. 10 mL 0.1 mol/L CH3COOH溶液与5 mL 0.2 mol/L NaOH溶液混合:c(Na+)=c(CH3COO)>c(OH)>c(H+)
D. 10 mL 0.5 mol/L CH3COONa溶液与6 mL 1 mol/L盐酸混合:c(Cl)>c(Na+)>c(OH)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是中学常见的四种短周期元素,其原子序数依次增大,且原子核外最外层电子数都不少于2,X与W的最外层电子数相等。四种元素的单质均能在氧气中燃烧,生成四种相对分子质量都大于26的氧化物,其中有两种氧化物能溶于稀硫酸,三种氧化物能溶于烧碱溶液。四种元素的单质所形成的混合物有如下性质:
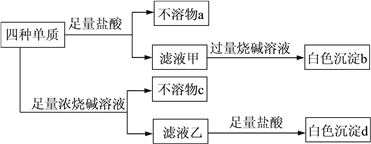
下列说法正确的是
A.原子半径:X>Y>Z>W
B.简单的气态氢化物的热稳定性:W>X
C.最高价氧化物对应水化物的碱性:Z>Y
D.X和W组成的化合物常作砂纸、砂轮的磨料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W为原子序数依次增大的四种短周期主族元素,X原子的最外层电子数是其内层电子数的2倍,W+与Y2-具有相同的电子层结构。下列说法正确的是
A.Y与氢元素所形成的化合物分子中只含有极性键
B.W2Y、W2Y2中阴、阳离子个数比均为1∶2
C.Z的最高价氧化物对应的水化物的酸性比X的强
D.将XY2通入W单质与水反应后的溶液中,生成的盐只有一种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com