
【题目】某同学做浓度对化学反应速率的影响的实验时,将3支试管分别编号为①②③,并按下表中物质的量进行实验,记录下的时间数据是16 s、28 s、33 s。请将3个数据填入下面的适当位置,并写出实验结论。

(1)将对应①、②、③的时间分别写出:
(a)________,(b)________,(c)________。
(2)实验结论:______________________________________________。
(3)写出反应的化学方程式:______________________________。
【答案】 33 s 28 s 16 s 反应物浓度越大,反应速率越快 Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O
【解析】(1)图表中主要是改变了反应物的浓度,从而对反应速率产生了影响,浓度越大反应速率越大,反应物浓度①<②<③,则反应③速率最大,时间最短,反应①速率最小,时间最长,因此答案是33 s;28 s;16 s。
(2)对于一个化学反应,在其他条件不变时,改变反应物浓度,对反应速率的影响是:浓度越大反应速率越大。故答案是:反应物浓度越大,反应速率越快。
(3)Na2S2O3溶液和稀硫酸反应生成单质硫、二氧化硫和水,反应的化学方程式是:Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O。


科目:高中化学 来源: 题型:
【题目】下列热化学方程式正确的是( )
A. 甲烷的燃烧热为890.3 kJ·mol-1,则甲烷燃烧热的热化学方程式可表示为CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1
B. 将0.5 mol N2和1.5 mol H2置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为N2(g)+3H2(g)![]() 2NH3(g) ΔH=-38.6 kJ·mol-1
2NH3(g) ΔH=-38.6 kJ·mol-1
C. 已知在120 ℃、101 kPa下,1 g H2燃烧生成水蒸气放出121 kJ热量,其热化学方程式为H2(g)+![]() O2(g)===H2O(g) ΔH=-242 kJ·mol-1
O2(g)===H2O(g) ΔH=-242 kJ·mol-1
D. 25 ℃、101 kPa时,强酸与强碱的稀溶液发生中和反应的中和热为57.3 kJ·mol-1,硫酸溶液与氢氧化钾溶液反应的热化学方程式为H2SO4(aq)+2KOH(aq)===K2SO4(aq)+2H2O(l) ΔH=-57.3 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用惰性电极电解下列溶液,一段时间后,再加入一定质量的另一物质中(括号内),溶液能与原来溶液完全一样的是
A.CuSO4[Cu(OH)2]B.NaOH [NaOH]C.NaCl [盐酸]D.AgNO3[Ag2O]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了人类的可持续发展,我们应综合利用资源.保护环境,跟自然 和谐相处:
(1)科学家研制出有“自我修复能力”的塑料.塑料属于(选填“无机”、“合成”或“复合”)材料,为我们到来了方便,但废弃塑料处理不当会对环境造成不利的影响,人们把废弃塑料给环境带来的危害称为“”,发电厂是利用垃圾焚烧产生的转变为电能.
(2)发射“嫦娥三号”的长三甲火箭燃料是偏二甲肼(X),反应的化学方程式为:X+2N2O4=3N2+2CO2+4H2O,则X的化学式为
A.H2
B.CH4
C.C2H8N
D.C2H8N2
(3)2014年3月22日是第二十二个“世界水日”,它的主题是“水与能源”.关于水的知识有下列话题,请按要求填空: ①自来水生产过程中,可用方法除去水中不溶性杂质.
②在生产生活中水是最常用的溶剂,实验室用蔗糖配制一定溶质质量分数的溶液时,可能涉及以下操作: 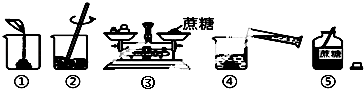
Ⅰ、如图操作中有错误的是(填序号).
Ⅱ、改正错误后,表示正确的操作顺序是(填序号).
A.⑤②①③④B.⑤①②③④C.⑤③②④①D.⑤③①④②
Ⅲ、保护水环境、珍爱水资源,是每个公民应尽的责任和义务.下列做法不利于保护水资源的是(填序号).
A.大量使用化肥农药 B.工业废水处理达标后再排放
C.使用含磷洗衣粉 D.生活污水直接排放.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】50 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
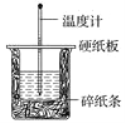
(1)从实验装置上看,图中尚缺少的一种玻璃仪器是________。
(2)烧杯间填满碎纸条的作用是________。
(3)大烧杯上如不盖硬纸板,求得的中和热数值____________(填“偏大”、“偏小”)。
(4)该实验常用0.50 mol·L-1HCl和0.55 mol·L-1NaOH溶液各50 mL进行实验,其中NaOH溶液浓度大于盐酸浓度的作用是________,当室温低于10 ℃时进行实验,对实验结果会造成较大的误差,其原因是______________________________________。
(5)实验中改用60 mL 0.50 mol·L-1盐酸与50 mL 0.50 mol·L-1NaOH溶液进行反应,与上述实验相比,所求得的中和热________(填“相等”或“不相等”),(1分)简述理由: _____________________________。
(6)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热ΔH将________(填“偏大”、“偏小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度和压强下,把装有NO和 NO2的混合气体的试管倒立于水中,充分反应后,试管内气体的体积缩小为原气体体积的3/5,则原混合气体中NO和NO2的体积比为( )
A.2:3 B.3:2 C. 5:3 D.3:5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业废水中常含有一定量的Cr2O72—和CrO42—,它们会对人类及生态系统产生很大的危害,必须进行处理。下面是一种处理方法的工业流程:

其中第①步存在平衡:2CrO42-(黄色)+2H+![]() Cr2O72-(橙色)+H2O
Cr2O72-(橙色)+H2O
下列说法正确的是( )
A. 反应②中还原1mol Cr2O72—,需要6 mol的Fe2+
B. 改变反应①的平衡体系中c(H+)浓度,溶液颜色无明显变化
C. 若2v (Cr2O72-) =v (CrO42-),说明反应①达平衡状态
D. FeSO4溶液呈酸性的原因是Fe2++ 2H2O ![]() Fe(OH) 2↓+ 2H+
Fe(OH) 2↓+ 2H+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com