
| A. | 反应现象相同,反应类型相同 | B. | 反应现象相同,反应类型不同 | ||
| C. | 反应现象不同,反应类型相同 | D. | 反应现象不同,反应类型不同 |
分析 将丙烯通入溴水中,则丙烯和溴发生加成反应生成CH3CHBrCH2Br,不溶于水;丙烯通入溴的四氯化碳溶液中,丙烯和溴发生加成反应生成CH3CHBrCH2Br,易溶于四氯化碳,据此分析.
解答 解:将丙烯通入溴水中,则丙烯和溴发生加成反应生成CH3CHBrCH2Br,不溶于水,故和溴水反应后所得的溶液分层:水在上层,油状的CH3CHBrCH2Br在下层,均无色;丙烯通入溴的四氯化碳溶液中,丙烯和溴发生加成反应生成CH3CHBrCH2Br,溶液褪色,易溶于四氯化碳,故溶液互溶不分层,故两反应类型相同,但现象不同,故选C.
点评 本题考查了烯烃和溴的反应,应注意的是CH3CHBrCH2Br,不溶于水,但易溶于四氯化碳.


科目:高中化学 来源: 题型:选择题
| A. | H2S和CS2分子都是含极性键的极性分子 | |
| B. | 在石墨晶体中,共价键与碳原子的个数比为2:3 | |
| C. | 熔点由高到低的顺序是:金刚石>碳化硅>晶体硅 | |
| D. | PCl3和BCl3分子中所有原子的最外层都达到8电子稳定结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

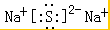 ,温度高于150℃完全分解得到固体Y和固体Z的化学方程式为4Na2SO3$\frac{\underline{\;高温\;}}{\;}$3Na2SO4+Na2S;
,温度高于150℃完全分解得到固体Y和固体Z的化学方程式为4Na2SO3$\frac{\underline{\;高温\;}}{\;}$3Na2SO4+Na2S;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | vA=0.5mol/L•s | B. | vB=0.6mol/L•s | C. | vC=0.4mol/L•s | D. | vD=2mol/L•min |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 过碳酸钠(2Na2CO3•3H2O2)是一种集洗涤、漂白、杀菌于一体的氧系漂白剂,易分解.可用纯碱与H2O2反应制取,反应方程式为:2Na2CO3(aq)+3H2O2(aq)?2Na2CO3•3H2O2(s)△H<0,如图是制取过碳酸钠 的示意图,步骤如下
过碳酸钠(2Na2CO3•3H2O2)是一种集洗涤、漂白、杀菌于一体的氧系漂白剂,易分解.可用纯碱与H2O2反应制取,反应方程式为:2Na2CO3(aq)+3H2O2(aq)?2Na2CO3•3H2O2(s)△H<0,如图是制取过碳酸钠 的示意图,步骤如下查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 )具有超强阻隔性能,可作为保鲜食品的包装材料.它是由CCl2=CH2(写结构简式)发生加聚反应生成的.
)具有超强阻隔性能,可作为保鲜食品的包装材料.它是由CCl2=CH2(写结构简式)发生加聚反应生成的.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com