

分析 乙烯与HCl加成反应生成A为CH3CH2Cl,A水解生成B为CH3CH2OH,B氧化生成乙醛,乙醛与HCN发生加成反应生成C为CH3CH(OH)CN,C酸化生成乳酸,然后结合有机物的结构与性质来解答.
解答 解:乙烯与HCl加成反应生成A为CH3CH2Cl,A水解生成B为CH3CH2OH,B氧化生成乙醛,乙醛与HCN发生加成反应生成C为CH3CH(OH)CN,C酸化生成乳酸.
(1)C的结构简式为:CH3CH(OH)CN,故答案为:CH3CH(OH)CN;
(2)①生成A的反应方程式为:CH2=CH2+HCl→CH3CH2Cl,
②B→CH3CHO的反应方程式为:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O,
③实验室制乙烯的反应方程式为:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O,
故答案为:CH2=CH2+HCl→CH3CH2Cl;2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O;CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O.
点评 本题考查有机物的推断与合成,涉及烯烃、卤代烃、醇、醛等性质与转化,注意根据有机物结构简式与反应条件分析,注意对基础知识的理解掌握.


 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源: 题型:解答题
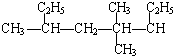 3,5,5-三甲基辛烷
3,5,5-三甲基辛烷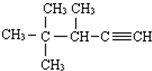 3,4,4-三甲基-1-戊炔
3,4,4-三甲基-1-戊炔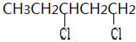 1,3-二氯戊烷
1,3-二氯戊烷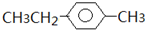 1-甲基-4-乙基苯
1-甲基-4-乙基苯
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
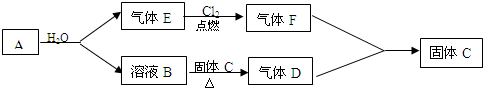

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 安全气囊中原料的配比为$\frac{n(Na{N}_{3})}{n(KN{O}_{3})}$=5 | |
| B. | 若在标准状况下,产生44.8L N2,则有0.25mol KNO3参与反应 | |
| C. | 上述复分解反应发生速度很快,瞬间能产生大量气体 | |
| D. | 根据安全气囊打开时产生气体的体积(标准状况),可大致计算出气囊中原料的质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
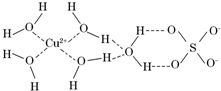 第四周期的许多金属能形成配合物.科学家通过X射线测得胆矾结构示意图可简单表示如下:
第四周期的许多金属能形成配合物.科学家通过X射线测得胆矾结构示意图可简单表示如下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在共价化合物中一定含有共价键 | |
| B. | 由非金属元素组成的化合物一定是共价化合物 | |
| C. | 含有离子键的化合物一定是离子化合物 | |
| D. | 双原子单质分子中的共价键一定是非极性键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com