
【题目】下列说法正确的是
A.等质量的甲烷、乙烯、1,3—丁二烯分别充分燃烧,所耗用氧气的量依次减少
B.按系统命名法,化合物![]() 的名称为2—甲基—4—乙基戊烷
的名称为2—甲基—4—乙基戊烷
C.苯酚、水杨酸( )和苯甲酸都是同系物
)和苯甲酸都是同系物
D.三硝基甲苯的分子式为C7H3N3O6
科目:高中化学 来源: 题型:
【题目】对于苯乙烯(![]() )的下列叙述:
)的下列叙述:
①所有的原子不可能共面 ②可溶于水 ③可溶于苯中 ④能使酸性KMnO4溶液褪色
⑤可发生加聚反应 ⑥1mol苯乙烯与H2反应最多消耗4molH2。其中完全正确的一组是( )
A. ①②④⑤B. ③④⑤⑥C. ①③⑤⑥D. ②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海冰是海水冻结而成的咸水冰,海水冻结时,部分来不及流走的盐分(设以NaCl为主)以卤汁的形式包裹在冰晶之间,形成“盐泡”,其大致结构如图所示。若海冰的冰龄达到1年以上,则融化后的水为淡水。用NA表示阿伏加德罗常数的值,设冰的密度为0.9g/cm3。下列叙述正确的是

A.海冰内层“盐泡”越少,密度越大
B.海冰冰龄越短,内层的“盐泡”越少
C.冰的密度比水小是因为在固态冰中水分子间以氢键结合,排列更规整
D.每含1mol H2O的海冰内就有2×105 NA个NaCl分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种芳纶纤维的拉伸强度比钢丝还高,广泛用作防护材料。其结构片段如下图
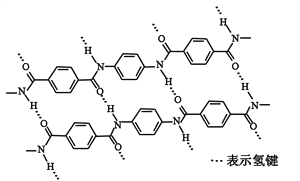
下列关于该高分子的说法正确的是
A. 完全水解产物的单个分子中,苯环上的氢原子具有不同的化学环境
B. 完全水解产物的单个分子中,含有官能团―COOH或―NH2
C. 氢键对该高分子的性能没有影响
D. 结构简式为:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O,如图所示,将少量试剂分别放入培养皿中的相应位置,实验时将浓盐酸滴在KClO3晶体上,并用表面皿盖好。下表中由实验现象得出的结论完全正确的是( )
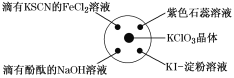
选项 | 实验现象 | 结论 |
A | 滴有KSCN的FeCl2溶液变红 | Cl2具有还原性 |
B | 滴有酚酞的NaOH溶液褪色 | Cl2具有酸性 |
C | 紫色石蕊溶液先变红后褪色 | Cl2具有漂白性 |
D | KI淀粉溶液变成蓝色 | Cl2具有氧化性 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知乙酸乙酯与NaOH溶液在加热条件下发生水解,生成醋酸钠和乙醇。而1mol![]() 与NaOH溶液发生反应时最多消耗3 mol NaOH。五倍子是一种常见的中草药,其有效成分为X。在一定条件下X可分别转化为Y、Z。
与NaOH溶液发生反应时最多消耗3 mol NaOH。五倍子是一种常见的中草药,其有效成分为X。在一定条件下X可分别转化为Y、Z。
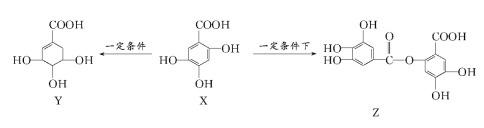
下列说法错误的是( )
A. 1molZ最多能与6molNaOH发生反应
B. 1molX最多能与2molBr2发生取代反应
C. Y分子结构中有2个手性碳原子
D. Y能发生加成、取代、消去、氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ni2+与丁二酮肟生成鲜红色丁二酮肟镍沉淀,该反应可用于检验Ni2+。
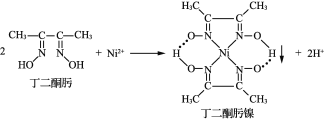
(1)Ni2+基态核外电子排布式为___________。
(2)1mol丁二酮肟分子中含有σ键的数目为______mol。
(3)丁二酮肟镍分子中碳原子的杂化轨道类型为_____。
(4)Ni(CO)4是一种无色液体,沸点为43℃,熔点为-19.3 ℃。Ni(CO)4的晶体类型是____。
(5)与CO互为等电子体的二价阴离子为_____,Ni(CO)4中Ni与CO的C原子形成配位键,不考虑空间构型,Ni(CO)4的结构可用示意图表示为_____。
(6)下列离子的VSEPR模型与离子的空间立体构型一致的是_______。
A.SO32- B.ClO4- C.NO2- D.ClO3-
(7)最近发现,只含镁、镍和碳三种元素的晶体竟然也具有超导性。鉴于这三种元素都是常见元素,从而引起广泛关注。该新型超导晶体的一个晶胞如图所示,则该晶体的化学式为______
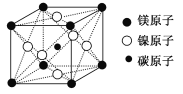
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝的利用成为人们研究的热点,是新型电池研发中重要的材料。
(1)通过以下反应制备金属铝。
反应1:Al2O3(s)+AlCl3(g)+3C(s)=3AlCl(g)+3CO(g);ΔH1=akJ·mol-1
反应2:Al2O3(s)+3C(s)=2Al(l)+3CO(g);ΔH2=bkJ·mol-1
反应3:3AlCl(g)=2Al(l)+AlCl3(g);ΔH3
试比较a、b的大小,并说明理由:a___b,理由是___。
(2)在高温条件下进行反应:2Al(l)+AlCl3(g)![]() 3AlCl(g)。
3AlCl(g)。
①向图1所示的等容积A、B密闭容器中加入足量的Al粉,再分别充入1molAlCl3(g),在相同的高温下进行反应。图2表示A容器内的AlCl3(g)体积分数随时间的变化图,在图2中画出B容器内AlCl3(g)体积分数随时间的变化曲线。___
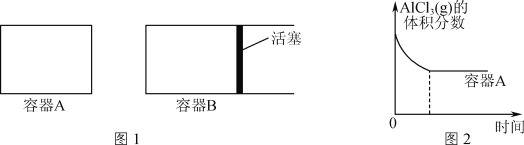
②1100℃时,向2L密闭容器中通入3molAlCl(g),发生反应:3AlCl(g)![]() 2Al(l)+AlCl3(g)。已知该温度下AlCl(g)的平衡转化率为80%,则该反应的平衡常数K=___。
2Al(l)+AlCl3(g)。已知该温度下AlCl(g)的平衡转化率为80%,则该反应的平衡常数K=___。
③加入3molAlCl(g),在不同压强下发生反应,温度对产率的影响如图3所示。此反应选择温度为900℃的原因是___。研究表明,当温度达到2500℃以上时,图中曲线重合,试分析可能原因___。
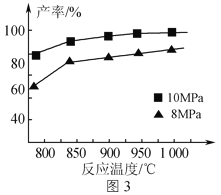
(3)用铝制作的快速放电铝离子二次电池的原理如图4所示。该电池充电时,阴极的电极反应式为___。
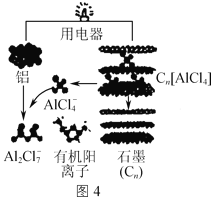
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】槟榔碱在医疗上常用于治疗青光眼,其一种合成路线如图:
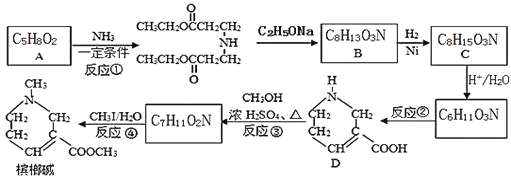
已知:Ⅰ.不饱和化合物与氨(NH3)或胺(R﹣NH2)反应能生成新的胺类化合物如:R1﹣CH=CH2+R2﹣NH2![]() R1﹣CH2﹣CH2﹣NH﹣R2
R1﹣CH2﹣CH2﹣NH﹣R2
Ⅱ.![]() +
+![]()
![]()
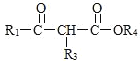 + R2OH
+ R2OH
(1)B的含氧官能团名称为_______________。
(2)反应②④的反应类型分别为______________、______________。
(3)反应③的化学方程式为___________________。
(4)A、C的结构简式分别为_____________、_______________。
(5)A的同分异构体中满足下列条件的有 _______ 种(不考虑立体异构)。
a.含有能与NaHCO3溶液反应放出CO2气体的官能团;
b.能使溴的CCl4溶液褪色。
(6)结合题中信息,以乙二醇为主要原料,其他无机试剂任选,写出合成![]() 的最简单路线____________。
的最简单路线____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com