
 �ȼҵ�Ե�⾫�Ʊ���ʳ��ˮ�ķ�����ȡ�������������ռ���ȵĺ������ε�ϵ�л�����Ʒ��ͼ2�����ӽ���Ĥ�����ʳ��ˮ��ʾ��ͼ��ͼ�е����ӽ���Ĥֻ����������ͨ�������������գ�
�ȼҵ�Ե�⾫�Ʊ���ʳ��ˮ�ķ�����ȡ�������������ռ���ȵĺ������ε�ϵ�л�����Ʒ��ͼ2�����ӽ���Ĥ�����ʳ��ˮ��ʾ��ͼ��ͼ�е����ӽ���Ĥֻ����������ͨ�������������գ����� ��1����⾫�Ʊ���ʳ��ˮ�����������������ռ
��2�������ӽ���Ĥֻ��������ͨ���������Ӻ����岻��ͨ����
��3����ⱥ��ʳ��ʱ����������Cl-��OH-�ŵ磬Cl-�ķŵ�����ǿ��OH-�����������ķ���ʽΪ��2Cl--2e-�TCl2����������2H++2e-�TH2����H2��NaOH��������NaOH��Һ�ij���Ϊd��Cl2�����������Ʊ���ʳ��ˮ���������룻
��� �⣺��1����⾫�Ʊ���ʳ��ˮ�ķ�����ȡ�������������ռ��Ӧ�����ӷ���ʽΪ��2Cl-+2H2O$\frac{\underline{\;ͨ��\;}}{\;}$2OH-+H2��+Cl2����
�ʴ�Ϊ��2Cl-+2H2O$\frac{\underline{\;ͨ��\;}}{\;}$2OH-+H2��+Cl2����
��2�������ӽ���Ĥֻ��������ͨ���������Ӻ����岻��ͨ������ʯī���缫��ⱥ���Ȼ���ʱ�������������ӷŵ�������������������ͨ�������ӽ���Ĥ�����������������������������������ϲ�����ը����������������Һ��Ӧ�����Ȼ��ơ��������ƶ�������ȡ���������Ʋ�����
�ʴ�Ϊ����ֹ�������ɵ��������������ɵ��������Ʒ�Ӧ��ʹ��Ʒ��������ֹ�������ɵ��������������ɵ�������Ӧ����Ӧ��������ȫ�¹ʣ�
��3�������������������ӷŵ�����������ˮ����ƽ�������������������Ũ��������������������Һ��NaOH��Һ�ij���Ϊd��
Cl2������������װ��ͼ������֪���Ʊ���ʳ��ˮ���������룬������Ϊa��
�ʴ�Ϊ��a��d��
���� ���⿼���˵��ԭ���ķ������缫�����жϷ�������ѧ����ʽ��д�ȣ���Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
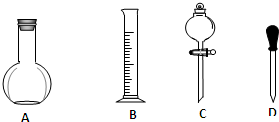 ʵ������Ҫ��NaOH��������0.1mol/LNaOH��Һ450mL����Ũ��������0.5mol/L��������Һ500mL��������������Һ����������ش��������⣮
ʵ������Ҫ��NaOH��������0.1mol/LNaOH��Һ450mL����Ũ��������0.5mol/L��������Һ500mL��������������Һ����������ش��������⣮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
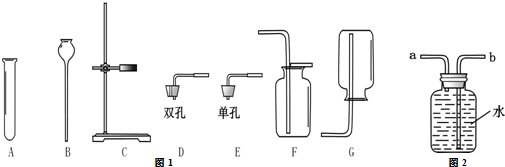
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
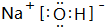 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ڿ������ܺܿ��γ�����Ĥ | |
| B�� | ����ʧȥ�������������������Ž����� | |
| C�� | ���������۵������ | |
| D�� | �������������Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2H2��g��+O2��g��=2H2O ��l����H=-571.6 kJ/mol��ȼ���ȣ� | |
| B�� | NaOH��aq��+CH3COOH��aq��=CH3COONa��aq��+H2O��l����H=-57.3kJ/mol���к��ȣ� | |
| C�� | H2O ��g��=H2��g��+$\frac{1}{2}$O2��g����H=-242 kJ/mol ����Ӧ�ȣ� | |
| D�� | C��s��+O2�� g ��=CO2��g����H=-393.5 kJ/mol����Ӧ�ȣ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��״���£�22.4 L�����к���NA�����ʷ��� | |
| B�� | 1 mol Cl2�μӷ�Ӧת�Ƶ�����һ��Ϊ2NA | |
| C�� | NA��NO2��92g N2O4������ͬ����ԭ���� | |
| D�� | ��״����22.4L CO�볣����44gCO2����̼ԭ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ʯ���� | B�� | ��Ʒ��� | C�� | �����ڻ� | D�� | ʳ�︯�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com