
【题目】某原电池总反应离子方程式为:2Fe3+ +Fe = 3Fe2+,能实现该反应的原电池是
A. 电极材料为铁和锌,电解质溶液为Fe2(SO4)3溶液
B. 电极材料都是铁,电解质溶液为Fe(NO3)2溶液
C. 电极材料为铁和石墨,电解质溶液为FeCl3溶液
D. 电极材料为铁和石墨,电解质溶液为FeCl2溶液
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】已知:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H1=﹣Q1 kJ·mol﹣1
2H2(g)+O2(g)═2H2O(l)△H3=﹣Q2 kJ·mol﹣1 取体积比2:3的甲烷和氢气的混合气体11.2L(标准状况下),经完全燃烧后恢复至室温,则放出的热量为( )
A. 0.4Q1+0.15Q2 B. 0.2Q1+0.05Q2 C. 0.2Q1+0.15Q2 D. 0.2Q1+0.3Q2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2和I2在一定条件下能发生反应:H2(g)+I2(g)![]() 2HI(g) ΔH=-a kJ·mol-1
2HI(g) ΔH=-a kJ·mol-1
已知:
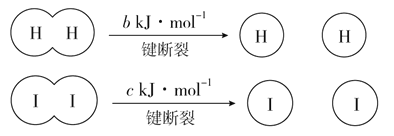
(a、b、c均大于零)
下列说法不正确的是
A. 反应物的总能量高于生成物的总能量
B. 断开1 mol H—H键和1 mol I—I键所需能量大于断开2 mol H—I键所需能量
C. 断开2 mol H—I键所需能量约为(c+b+a)kJ
D. 向密闭容器中加入2 mol H2和2 mol I2,充分反应后放出的热量小于2a kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,将2molA和3molB充入—密闭容器中,发生反应:aA(g)+B (g) ![]() C(g)+D(g) 5分钟后达到平衡。己知各物质的平衡浓度的关系为[A]a[B]=[C][D],若在温度不变情况下将容器的体积扩大为原来的10倍,并A的转化率不发生变化,则B的转化率为
C(g)+D(g) 5分钟后达到平衡。己知各物质的平衡浓度的关系为[A]a[B]=[C][D],若在温度不变情况下将容器的体积扩大为原来的10倍,并A的转化率不发生变化,则B的转化率为
A. 60% B. 24% C. 4% D. 40%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于合金的叙述中正确的是( )
A. 合金是由两种或多种金属熔合而成的
B. 日常生活中用到的5角硬币属于铜合金
C. 合金在任何情况下都比单一金属性能优良
D. 钢不属于合金
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将24.4 g NaOH固体溶于水配成100 mL溶液,其密度为1.219 g·mL-1。
(1)该溶液中NaOH的物质的量浓度为________。
(2)该溶液中NaOH的质量分数为________。
(3)从该溶液中取出10 mL,溶液的密度为________,含NaOH的物质的量为________。
(4)将取出的10 mL溶液加水稀释到100 mL,稀释后溶液中NaOH的物质的量浓度为________。
(5)标准状况下,1.7 g NH3标准状况下________ L H2S含有相同数目的氢原子。
(6)某气体氧化物的化学式为RO2,标准状况下,1.28 g该氧化物的体积为448 mL,则该氧化物的摩尔质量为________,R的相对原子质量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.1mol两种气体烃组成的混合气完全燃烧后得3.36L(标况)CO2和3.6g水,对于组成判断正确的是( )
A.一定有甲烷B.一定有乙烯C.一定没有甲烷D.一定没有乙烷
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com