
ĶعżŅŌĻĀĶ¾¾¶æÉŅŌŗĻ³É¾ßÓŠµ¼µēŠŌµÄøß·Ö×Ó²ÄĮĻF£ŗ

ŅŃÖŖ£ŗ
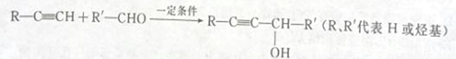
(1)ĪļÖŹCĖłŗ¬¹ŁÄÜĶŵÄĆū³ĘĪŖ____________£¬ŹŌ¼ĮXµÄ½į¹¹¼ņŹ½ŹĒ___________”£
(2)Ģõ¼žYŹĒ________________
(3)ĒėŠ“³ö·“Ó¦¢ŚµÄ»Æѧ·½³ĢŹ½£ŗ__________________
(4)CÓėH2ŅŌ1£ŗ2·“Ó¦ĖłµĆ²śĪļµÄĻµĶ³ĆüĆūŹĒ________________
(5)·“Ó¦¢ŽµÄ»Æѧ·“Ó¦ĄąŠĶĪŖ________£¬·“Ó¦¢ŻµÄ»Æѧ·½³ĢŹ½_____________”£
(6)·“Ó¦¢Ł³£ÓƱ„ŗĶŹ³ŃĪĖ®“śĢęH2O£¬ĘäÄæµÄŹĒ_________________
(7)Š“³ö·ūŗĻĻĀĮŠĢõ¼žŌŚBµÄĖłÓŠĶ¬·ÖŅģ¹¹Ģå_______________”£
¢ŁÄÜÓėŅų°±ČÜŅŗ·“Ó¦ ¢ŚŗĖ“Ź²ÕńĒāĘ×ÓŠ3øöĪüŹÕ·å
(8)²ĪÕÕÉĻŹöŗĻ³ÉŠÅĻ¢£¬ŅŌ±ūČ²”¢¼×Č©ŗĶŅŅĖįĪŖŌĮĻ£ØĪŽ»śŹŌ¼ĮČĪŃ”£©Éč¼ĘĀ·ĻßŗĻ³ÉŅŅĖį”Ŗ
 _________________ӣ
_________________ӣ
ŗĻ³ÉĀ·Ļߏ¾ĄżČēĻĀ£ŗCH2=CH2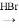 CH3CH2Br
CH3CH2Br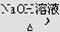 CH3CH2OH
CH3CH2OH
 æŚĖćĢāĢģĢģĮ·ĻµĮŠ“š°ø
æŚĖćĢāĢģĢģĮ·ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģ½ĖÕŹ”ÄĻĶØŹŠøßČżøßæ¼Č«ÕęÄ£Äā£Ø¶ž£©»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ijӊ»śĪļŹĒŅ»ÖÖŅ½Ņ©ÖŠ¼äĢ壮Ęä½į¹¹¼ņŹ½ČēĶ¼ĖłŹ¾”£ĻĀĮŠÓŠ¹ŲøĆĪļÖŹµÄĖµ·ØÕżČ·µÄŹĒ£Ø £©
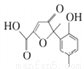
A. øĆ»ÆŗĻĪļ·Ö×ÓÖŠ²»ŗ¬ŹÖŠŌĢ¼Ō×Ó
B. øĆ»ÆŗĻĪļÓėNaHCO3ČÜŅŗ×÷ÓĆÓŠCO2ĘųĢå·Å³ö
C. 1 moløĆ»ÆŗĻĪļÓė×ćĮæäåĖ®·“Ó¦£¬ĻūŗÄ2 mol Br2
D. ŌŚŅ»¶ØĢõ¼žĻĀ£¬øĆ»ÆŗĻĪļÓėHCHOÄÜ·¢ÉśĖõ¾Ū·“Ó¦
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģÄŚĆɹŰüĶ·ŹŠøßČżĻĀѧʌµŚŅ»“ĪÄ£Äāæ¼ŹŌĄķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗ¼ņ“šĢā
ĄūÓĆŠæĆĢøɵē³ŲÄŚµÄŗŚÉ«¹ĢĢåĖ®½žŗóµÄĢ¼°üĀĖŌü(ŗ¬MnO2”¢C”¢Hg2+µČ£©ÖĘČ”MnSO4 • H2O µÄŹµŃéĮ÷³ĢČēĻĀ£ŗ
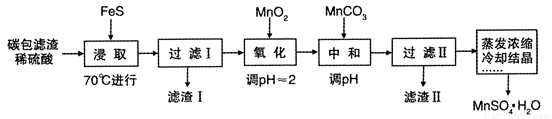
ŅŃÖŖ:25”ꏱ£¬¼øÖÖĮņ»ÆĪļµÄČܶȻż³£ŹżČēĻĀ:
ĪļÖŹ | FeS | MnS | HgS |
ČܶȻż | 5.0”Įl0-18 | 4.6”Įl0-14 | 2.2”Įl0-54 |
25”ꏱ£¬²æ·Ö½šŹōŃōĄė×ÓŅŌĒāŃõ»ÆĪļŠĪŹ½³ĮµķŹ±ČÜŅŗµÄpHČēĻĀ±ķĖłŹ¾:
³ĮµķĪļ | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 |
æŖŹ¼³ĮµķµÄpH | 2.7 | 7.6 | 8.3 |
ĶźČ«³ĮµķµÄpH | 3.7 | 9.7 | 9.8 |
£Ø1£©ÉĻŹöĮ÷³ĢÖŠ£¬Õō·¢ŹµŃé²Ł×÷Ź±ÓƵ½µÄ¹čĖįŃĪ²ÄÖŹµÄŅĒĘ÷ÓŠ______________”£
£Ø2£©ŌŚ¼ÓČČĢõ¼žĻĀ”°½žČ””±£¬ĘäŌŅņŹĒ__________________£»½žČ”Ź±Éś³ÉMnSO4ŗĶFe2(SO4)3µÄ»Æѧ·½³ĢŹ½ĪŖ__________________________”£
£Ø3£©ĀĖŌüIµÄ³É·ÖĪŖMnO2”¢CŗĶ____________(Ģī»ÆѧŹ½£©£»Čō½žČ”·“Ó¦ŌŚ25”ꏱ½ųŠŠ£¬FeS×ćĮ棬Ōņ³ä·Ö½žČ”ŗóČÜŅŗÖŠµÄc(Hg2+)/C(Fe2+)= ____________(ĢīŹżÖµ£©”£
£Ø4£©”°Ńõ»Æ”±Ź±µÄĄė×Ó·½³ĢŹ½ĪŖ____________£»Ńõ»ÆŹ±æÉÓĆH2O2“śĢęMnO2£¬H2O2µÄµē×ÓŹ½ĪŖ_______”£
£Ø5£©ÖŠŗĶŹ±£¬Ó¦øƵ÷½ŚČÜŅŗpHµÄ·¶Ī§µ½____________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğ½Ī÷Ź”øßŅ»ĻĀѧʌµŚŅ»“ĪŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŅŃÖŖX”¢Y”¢ZČżÖÖÖ÷×åŌŖĖŲŌŚŌŖĖŲÖÜĘŚ±ķÖŠµÄĪ»ÖĆČēĶ¼ĖłŹ¾”£ÉčXµÄŌ×ÓŠņŹżĪŖa£¬ŌņĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
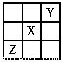
A. YµÄŌ×ÓŠņŹżæÉÄÜĪŖa£17
B. YÓėZµÄŌ×ÓŠņŹżÖ®ŗĶæÉÄÜĪŖ2a
C. ZµÄŌ×ÓŠņŹżæÉÄÜĪŖa£«31
D. X”¢Y”¢ZŅ»¶ØĪŖ¶ĢÖÜĘŚŌŖĖŲ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğ½Ī÷Ź”øßŅ»ĻĀѧʌµŚŅ»“ĪŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
øł¾ŻĻĀ±ķÖŠÓŠ¹Ų¶ĢÖÜĘŚŌŖĖŲŠŌÖŹµÄŹż¾Ż£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©
¢Ł | ¢Ś | ¢Ū | ¢Ü | ¢Ż | ¢Ž | ¢ß | ¢ą | ||
Ō×Ó°ė¾¶£Ø10©10 m£© | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 | |
Ö÷ŅŖ»ÆŗĻ¼Ū | ×īøß¼Ū | / | +2 | +1 | +5 | +7 | +1 | +5 | +3 |
×īµĶ¼Ū | ©2 | / | / | ©3 | ©1 | / | ©3 | / | |
A. ŌŖĖŲŌ×ÓŠņŹż¢Ü“óÓŚ¢ß B. ¢Ś¢ŪŗÅŌŖĖŲ²»æÉÄÜ“¦ÓŚĶ¬Ņ»ÖÜĘŚ
C. ¢ŻŗÅŌŖĖŲ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė® »ÆĪļµÄĖįŠŌ×īĒæ D. ¢ąŗÅŌŖĖŲŹĒ½šŹōŌŖĖŲ
»ÆĪļµÄĖįŠŌ×īĒæ D. ¢ąŗÅŌŖĖŲŹĒ½šŹōŌŖĖŲ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗĖÄ“ØŹ”¹ć°²”¢ĖģÄž”¢ÄŚ½”¢Ć¼É½ĖÄŹŠ2017½ģøßČżµŚ¶ž“ĪÕļ¶Ļæ¼ŹŌĄķ×Ū»ÆѧŹŌ¾ķ ĢāŠĶ£ŗŃ”ŌńĢā
H2C2O4ŹĒŅ»ÖÖ¶žŌŖČõĖį£¬H2C2O4ČÜŅŗÖŠø÷ŠĶĢåÅضČŌŚĘä×ÜÅضČÖŠĖłÕ¼±ČÖµ½ŠĘä·Ö²¼ĻµŹż£¬³£ĪĀĻĀijÅØ¶ČµÄH2C2O4ČÜŅŗÖŠø÷ŠĶĢå·Ö²¼ĻµŹżĖępHµÄ±ä»ÆČēĶ¼ĖłŹ¾£¬¾Ż“Ė·ÖĪö£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ

A. ĒśĻßa“ś±ķH2C2O4£¬ĒśĻßb“ś±ķC2O42-
B. ³£ĪĀĻĀ0.1mol/LµÄNaHC2O4ČÜŅŗĻŌĖįŠŌ
C. ³£ĪĀĻĀ£¬H2C2O4µÄµēĄėĘ½ŗā³£ŹżKa2=10-4..30
D. pH“Ó1.30”«4.30Ź±£¬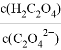 ĻČŌö“óŗó¼õŠ”
ĻČŌö“óŗó¼õŠ”
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğ¹ćĪ÷Ź”ÄĻÄžŹŠøßŅ»ĻĀѧʌµŚŅ»“ĪŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŹµŃéĢā
ĻĀĶ¼ŹĒø÷ÖÖ²»Ķ¬ĆܶȵÄĻõĖįÓėĢś·“Ó¦£ØĻąĶ¬ĪĀ¶Č£©Ź±Ö÷ŅŖ»¹Ō²śĪļµÄ·Ö²¼Ķ¼”£ĒėČĻÕę¶ĮĶ¼·ÖĪö£¬»Ų“šÓŠ¹ŲĪŹĢā”£

(1)ĻĀĮŠŠšŹöÖŠÕżČ·µÄŹĒ£ØĢīŠņŗÅ£©_______________”£
A.Ķ¼ÖŠŗį×ų±źŹĒĻõĖįµÄĆÜ¶Č£¬ĻõĖįµÄĆܶČŌ½“ó£¬ĘäÅضČŌ½Š””£
B.µ±»¹Ō¼ĮŗĶĪĀ¶ČĻąĶ¬Ź±£¬²»Ķ¬ÅØ¶ČµÄĻõĖį±»»¹ŌµÄ²śĪļ²»ŹĒµ„Ņ»µÄ£¬Ö»ŹĒŌŚÄ³ÅØ¶ČŹ±£¬ŅŌijÖÖ²śĪļĪŖÖ÷¶ųŅŃ”£
C.ĻõĖįµÄÅضČŌ½“󣬻¹Ō²śĪļÖŠNŌŖĖŲµĶ»ÆŗĻ¼Ū²śĪļŌ½ÉŁ
D.µ±ĻõĖįĆܶȓóÓŚ1.3g”¤cm-3Ź±£¬»¹Ō²śĪļÖ÷ŅŖĪŖNO”¢NO2
(2)“ÓĻĀĶ¼ÖŠŃ”ŌńŅĒĘ÷”¢Ņ©Ę·ŃéÖ¤ÓÉĢśŗĶ¹żĮæ1.36 g”¤cm-3ĻõĖį·“Ó¦²śÉśµÄĘųĢåÖŠŗ¬ÓŠNO£ØN2ŗĶO2µÄÓĆĮææÉ×ŌÓÉæŲÖĘ£¬¼ÓČČ×°ÖĆŗĶ¹Ģ¶Ø×°ÖĆŹ”ĀŌ£©
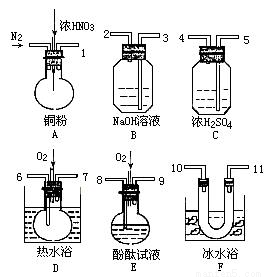
ŅŃÖŖ£ŗ¢ń.NO+NO2+2OH-=2NO2-+H2O
¢ņ.³£ĪĀĻĀ£¬NO2ÓėN2O4»ģŗĻ“ęŌŚ£¬ŌŚ0”ꏱ¼øŗõÖ»ÓŠĪŽÉ«µÄN2O4ŅŗĢå»ņ¾§Ģå“ęŌŚ”£
¢ŁŅĒĘ÷µÄĮ¬½ÓĖ³Šņ£Ø°“×ó”śÓŅĮ¬½Ó£¬Ģīø÷½ÓæŚµÄ±ąŗÅ£©ĪŖ______________”£
¢Ś·“Ó¦Ē°ĻČĶØČėN2£¬ÄæµÄŹĒ___________________”£
¢ŪČ·ČĻĘųĢåÖŠŗ¬µÄĻÖĻóŹĒ__________________”£
¢Ü×°ÖĆFµÄ×÷ÓĆŹĒ________________”£
¢ŻČō“ÓA³öĄ“µÄ»ģŗĻĘųĢåÖŠNO2”¢NOµÄĢå»ż·Ö±šĪŖV1mL”¢V2mL£ØV1”¢V2¾ł²»ĪŖ0£©£¬ĒŅ±¾Ģ××°ÖĆ×īÖÕÄܽ«µŖµÄŃõ»ÆĪļĶźČ«ĪüŹÕ£¬Ōņ×°ÖĆÖŠÖĮÉŁŠčŅŖ³åČėŃõĘųµÄĢå»żĪŖ£ŗ________mL£ØĻąĶ¬×“Ģ¬ĻĀ£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğ¹ćĪ÷Ź”ÄĻÄžŹŠøßŅ»ĻĀѧʌµŚŅ»“ĪŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠ½āŹĶŹĀŹµµÄĄė×Ó·½³ĢŹ½²»ÕżČ·µÄŹĒ
A£®Na·ÅČėĖ®ÖŠ£¬²śÉśĘųĢå£ŗ2Na + 2H2O £½ 2Na+ + 2OH£ + H2”ü
B£®FeCl3ČÜŅŗµĪŌŚµķ·Ūµā»Æ¼ŲŹŌÖ½ÉĻ£¬ŹŌÖ½±äĄ¶£ŗ2Fe3+ + 2I££½ 2Fe2+ + I2
C£®ĢśČÜÓŚĻ”ĻõĖį£¬ČÜŅŗ±ä»Ę£ŗ3Fe + 8H+ + 2NO3££½ 3Fe2+ + 2NO”ü+ 4H2O
D£®AlʬÖĆÓŚNaOHČÜŅŗÖŠ£¬²śÉśĘųĢå£ŗ2Al + 2OH£+ 2H2O £½ 2AlO2£ + 3H2”ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğø£½ØŹ””¢»Ż°²Ņ»ÖŠ”¢ČŖÖŻŹµŃé֊ѧøßŅ»ÉĻѧʌʌĩĮŖæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
ĻÖÓŠ°ĖÖÖĪļÖŹ£ŗ¢ŁĀĮ ¢ŚĀČĘų¢ŪA12O3 ¢ÜH2SO4 ¢ŻĻ”ĻõĖį¢ŽĻ”°±Ė®¢ßBa(OH)2¹ĢĢå¢ąA12(SO4)3Ēė°“ŅŖĒó»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ŹōÓŚµē½āÖŹµÄŹĒ______________£ØĢīŠņŗÅ£©”£
£Ø2£©m mol ¢ŚµÄÖŹĮæĪŖa g£¬Ōņb gøĆĘųĢåŌŚ±ź×¼×“æöĻĀµÄĢå»żĪŖ_______L (ÓĆm”¢a”¢b±ķŹ¾) ”£
£Ø3£©17.1g ¢ąČÜÓŚĖ®Åä³É500mLČÜŅŗ£¬ŌņČÜŅŗÖŠSO42”„µÄĪļÖŹµÄĮæÅضČĪŖ__________”£
£Ø4£©Š“³ö×īŹŹŅĖÖĘČ”Al(OH)3µÄĄė×Ó·½³ĢŹ½£ŗ__________________”£
£Ø5£©Į½ĪļÖŹČÜŅŗ¼ä·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖH++ OHØD £½ H2O£¬ĒėŠ“³öøĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ______________________”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com